« Cannabinoïdes synthétiques » : différence entre les versions
Aucun résumé des modifications |
Aucun résumé des modifications |
||
| Ligne 65 : | Ligne 65 : | ||
* '''les récepteur CB2''' sont principalement localisés au niveau du système immunitaire (notamment la rate). Leur stimulation aurait des effets anti-inflammatoires et immunosuppresseurs. | * '''les récepteur CB2''' sont principalement localisés au niveau du système immunitaire (notamment la rate). Leur stimulation aurait des effets anti-inflammatoires et immunosuppresseurs. | ||
La logique voudrait que les cannabinoïdes synthétiques vendus comme alternatives légales au cannabis (donc pour produire des effets psychotropes) soient préférentiellement agonistes des récepteurs CB1. Néanmoins, la course aux nouveaux produits conduit les distributeurs à mettre sur le marché des molécules pour lesquelles très peu d’informations sont disponibles. Ainsi, | La logique voudrait que les cannabinoïdes synthétiques vendus comme alternatives légales au cannabis (donc pour produire des effets psychotropes) soient préférentiellement agonistes des récepteurs CB1. Néanmoins, la course aux nouveaux produits conduit les distributeurs à mettre sur le marché des molécules pour lesquelles très peu d’informations sont disponibles. '''Ainsi, il n'est pas exclu que certains CS soient des agonistes préférentiels CB2, donc potentiellement immunosupresseurs'''. Les composés JWH-015<ref name=immuno1>[http://www.ncbi.nlm.nih.gov/pmc/articles/PMC1864948/ Lombard C, Nagarkatti M, Nagarkatti P. CB2 cannabinoid receptor agonist, JWH-015 triggers apoptosis in immune cells: Potential role for CB2 selective ligands as immunosuppressive agents. Clin Immunol. 2007;122(3):259–270]</ref>, JWH-133<ref name=immuno2>[http://www.jleukbio.org/content/82/3/532.full Xu H, Cheng CL, Chen M, et al. Anti-inflammatory property of the cannabinoid receptor-2-selective agonist JWH-133 in a rodent model of autoimmune uveoretinitis. J Leukoc Biol. 2007;82(3):532–541]</ref> et WIN-55,212-2<ref name=immuno3>[https://www.jstage.jst.go.jp/article/bpb/34/7/34_7_1090/_pdf Tanikawa T, Kurohane K, Imai Y. Regulatory effect of cannabinoid receptor agonist on chemokine-induced lymphocyte chemotaxis. Biol Pharm Bull. 2011;34(7):1090–1093] | ||
</ref> seraient concernés, et potentiellement tous les agonistes CB2 (AM-1241, AM-1221, HU-308, JWH-015, JWH-133, L-759,633, L-759,656, UR-144, 5F-UR-144, PB-22, 5F-PB-22, STS-135, etc...<ref name=immuno4>[http://www.psychonaut.com/reductions-des-risques/46833-ur-144-et-immunosuppression.html Psychonaut Forum : UR-144 et immunosuppression. Février 2013]</ref>. | |||
Version du 1 août 2013 à 17:43
Les cannabinoïdes synthétiques sont des molécules de synthèse qui agissent d'une façon proche de celle des cannabinoïdes végétaux, naturellement présents dans le cannabis (comme le THC)[1].
Ce sont principalement des agonistes des récepteurs cannabinoïdes. La plupart ont été développés à des fins thérapeutiques (analgésie), d’autres ont été synthétisés dans le but de créer des alternatives légales au cannabis.
Les cannabinoïdes synthètiques sont la classe la plus importante des nouveaux produits de synthèse. Sur les 73 nouvelles substances de synthèses reportées par le EMCDDA en 2012, 30 étaient des cannabinoïdes de synthèse. De 2008 à mai 2013, 84 cannabinoïdes de synthèse ont été reportés par le système d'alerte européen.[2]
Historique

Le premier « cannabis synthétique » se présentait sous forme d'un mélange de divers végétaux qui avaient été imprégnés de cannabinoïdes synthétiques. Il est apparu vers le milieu de années 2000 sous le nom de Spice[3] (Spice Gold, Spice Silver...). D'autres marques sont ensuite apparues (K2, Yucatan Fire, etc…). Ces produits n’ont véritablement gagné en popularité qu’à partir de la seconde moitié des années 2000.
Fin 2008, des analyses détectent dans ces mélanges la présence de cannabinoïdes de synthèse, notamment du CP-47,497-C8 et du JWH-018. Suite à des mesures visant à interdire ces composés dans plusieurs pays, les fabricants utiliseront alors de nouvelles molécules. En 2009 seront ainsi identifiés d’autres cannabinoïdes synthétiques comme le JWH-073, le JWH-019, le JWH-250, le JWH-398 ou encore le HU-210[4]. D’autres nouveaux composés seront régulièrement identifiés par la suite.
Composition
La plupart des poudres de cannabinoïdes synthétiques qui sont utilisés dans les «legal high» sont fabriqués en Chine puis sont expédiés en vrac par les réseaux de transport et de distribution légaux. Des expéditions de plusieurs kilos sont souvent interceptés par les autorités européennes, mais la pureté est rarement déterminés. Une étude en Corée du Sud a signalé des puretés entre 75% et 90% sur des échantillons de poudre en vrac. Les saisies européennes de poudres en vrac comprennent 54 kilogrammes de JWH-018 au Danemark (2012), 21 kilogrammes de JWH-018 en Finlande (2012) et 20 kilogrammes de AM-2201 en Espagne (2013).
Une fois en Europe, les produits sont mélangés à des herbes. Cette forme est principalement destinée à être fumée. Parmi les herbes utilisées comme support, on peut citer les espèces suivantes : Canavalia maritima, Nymphaea caerulea, Scutellaria nana, Pedicularis densiflora, Leonotis leonurus, Zornia latifolia, Nelumbo nucifera ou Leonurus sibiricus[3][4].
D'autre types de substances ont aussi été identifiées dans certains échantillons[4][5] :
- des dérivés d’acides gras ayant des effets proches des cannabinoïdes : oléamide, palmitamide, stéaramide
- des IMAO : harmine, harmaline
- un opioïde : le O-desmethyltramadol
- d’autres molécules dont certaines proviennent des plantes utilisées comme support et d’autres qui auraient été rajoutées
Aujourd’hui, les CS ne se trouvent plus uniquement au sein de mélanges d’herbes à fumer mais peuvent être obtenus sous forme de poudre isolée auprès de certains fournisseurs de RC. Ils peuvent également se trouver sous forme de résine (comme les marques Bang solid ou Afghan Insense) en réponse à la popularité croissante de la résine de cannabis dans de nombreux pays.
Chimie et noms des cannabinoïdes de synthèse
Beaucoup des cannabinoïdes de synthèse ont des noms de code qui ont trait à leur découverte. Dans certains cas, leur nom de code est issu des initiales du nom des scientifiques qui les a synthétisé la première fois : les composés "JWH" viennent de John W. Huffman, les composés "AM" viennent de Alexandros Makriyannis. Dans d'autres cas, ils peuvent provenir de l'entreprise où ils ont été synthétisés : la série «HU» vient de l'Université Hébraïque de Jérusalem.
D'autres peuvent avoir des noms de codes issus de leur nom chimique : APICA pour N-(1-adamantyl)-1-pentyl-1H-indole-3-carboxamide ou APINACA pour N-(1-adamantyl)-1-pentyl-1H-indazole-3-carboxamide
Plus récemment, ceux qui sont impliqués dans le commerce des "legal high" ont commencé à utiliser des noms de code qui ont probablement été choisis pour aider à commercialiser les produits. Par exemple, le AKB-48 est un autre nom utilisé du APINACA. AKB-48 est le nom d'un groupe populaire de filles japonaises qui a été comparé au groupe pop britannique «Spice Girls». Le cannabinoïde synthétique APICA est également appelé par le nom alternatif de "2NE1", qui est le nom d'un groupe de filles sud-coréenne qui a également été comparé aux Spice Girls. Enfin, le cannabinoïde synthétique XLR-11, semble avoir été nommé d'après le premier carburant liquide développé aux Etats-Unis pour une utilisation dans les avions.
Les cannabinoïdes de synthèse ont des structures variées. On peut distinguer [1][6][7][8] :
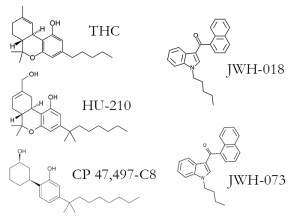
- Les naphthoylindoles :
JWH-007, JWH-015, JWH-018, JWH-019, JWH-073, JWH-081, JWH-098, JWH-116, JWH-122, JWH-149, JWH-182, JWH-193, JWH-198, JWH-200, JWH-210, JWH-398, JWH-424, AM-1220, AM-1221, AM-1235, AM-2201, AM-2232, MAM-2201
- Les benzoylindoles :
AM-630, AM-679, AM-694, AM-1241, AM-2233, RCS-4
- Les phénylacétylindoles :
JWH-167, JWH-203, JWH-250, JWH-251, JWH-320, RCS-8
- Les cyclohexylphénols :
CP-47,497, cannabicyclohexanol (ou CP-47,497-C8), CP-55,490, HU-308
- Les naphthylméthylindoles :
JWH-175, JWH-184
- Les naphthoylpyrroles :
JWH-030, JWH-147, JWH-307
- Les naphthylméthylindènes :
JWH-176
- Les adamantoylindoles :
AB-001, AM-1248
- Les cyclopropanoylindoles :
UR-144, 5F-UR-144 (ou XLR-11), A-834,735, A-796,260
- Les autres cannabinoïdes synthétiques :
HU-210, HU-211, WIN-55,212-2
Pharmacologie
Les cannabinoïdes (naturels ou synthétiques) agissent sur des récepteurs appelés récepteurs cannabinoïdes. Il en existe 2 types[9] :
- les récepteurs CB1 sont principalement localisés dans le système nerveux central. Leur stimulation induirait des effets euphorisants et anticonvulsivants.
- les récepteur CB2 sont principalement localisés au niveau du système immunitaire (notamment la rate). Leur stimulation aurait des effets anti-inflammatoires et immunosuppresseurs.
La logique voudrait que les cannabinoïdes synthétiques vendus comme alternatives légales au cannabis (donc pour produire des effets psychotropes) soient préférentiellement agonistes des récepteurs CB1. Néanmoins, la course aux nouveaux produits conduit les distributeurs à mettre sur le marché des molécules pour lesquelles très peu d’informations sont disponibles. Ainsi, il n'est pas exclu que certains CS soient des agonistes préférentiels CB2, donc potentiellement immunosupresseurs. Les composés JWH-015[10], JWH-133[11] et WIN-55,212-2[12] seraient concernés, et potentiellement tous les agonistes CB2 (AM-1241, AM-1221, HU-308, JWH-015, JWH-133, L-759,633, L-759,656, UR-144, 5F-UR-144, PB-22, 5F-PB-22, STS-135, etc...[13].
Prévalence
La prévalence de la consommation des cannabinoïdes synthétiques est largement inconnue. Un certain nombre d'études visant à examiner la prévalence de l'usage de produits "Spice et dérivés" ont été lancées mais leur couverture et leur représentativité reste limitée.
Il existe des différences notables entre les marchés européens et américains, cependant, certaines des données de prévalence les plus robustes viennent de l'étude US 2012 "Monitoring The futur", qui a identifié la prévalence d'utilisation des cannabinoïdes synthétiques à 8,8% et 11,3% pour les personnes âgées respectivement de 15/16 ans et 17/18 ans[14]. Un certain nombre d'enquêtes européennes signalent également les cannabinoïdes synthétiques, même si elles ne sont pas comparables à l’enquête US en raison des différentes méthodes, des cadres d'échantillonnage et de la terminologie.
Dans l'ensemble, toutefois, ces études déclarent de très faible prévalence. Le Royaume-Uni (Angleterre et Pays de Galles) a posé des questions sur l'utilisation du "Spice" dans deux enquêtes consécutives auprès des ménages et qui ont rapporté des niveaux de prévalence chez les adultes (16 à 64) de 0,2% en 2010/2011 et 0,1% en 2011/2012[15] [16]. En Espagne, une enquête nationale 2010 sur la consommation de drogues chez les étudiants âgés de 14 à 18 ans avec un échantillon de 25 000 personnes, a également identifié de faibles niveaux d'utilisation des produits «Spice» avec 1,1%, 0,8% et 0,4% rapporté respectivement à la prévalence de l'usage sur la vie, l'année dernière et le mois dernier.[17](7). En Allemagne, la ville de Francfort a étudié l'utilisation de mélanges d'herbes et de Spice parmi les étudiants âgés de 15 à 19 ans. Ils ont rapporté des niveaux utilisation lors de l vie de 6% en 2009 et 9% en 2010 [18]. Les élèves déclarant consommer du «Spice» étaient, pour la plupart, des consommateurs de cannabis expérimentés. Enfin, un certain nombre d'études chez des groupes particuliers (clubbers, internautes, etc) avec des échantillons non probabilistes ont généralement identifié des niveaux plus élevés d'utilisation des cannabinoïdes de synthèse que dans la population générale, par exemple avec l'étude de Mixmag 2011, a rapporté des niveaux de prévalence de 10,3% pendant la vie et 2,2% l'année passée.
Mode de consommation
Les cannabis synthétiques (Spice, K2, etc…) se présentent sous la forme de mélanges d'herbe. Ils sont destinés, comme le cannabis, à être fumés.
Les cannabinoïdes synthétiques peuvent aussi être obtenus sous forme purifiée (poudre). Ils peuvent alors être fumés (soit directement, dans un joint, soit en les dissolvant dans une solution qui sera pulvérisée sur un support végétal qui lui-même sera fumé) ou vaporisés. La voie orale est possible. Selon certains usagers, la voie nasale n’aurait pas d’intérêt, probablement en raison du caractère lipophile des CS. Pour la même raison, il semble difficile d’imaginer les injecter.
| « | j'ai goute un cannabioide 5f-AKB-48 pfff... ! Une puanteur de plastique et residus chimiques hallucinante ! J'ai fume un joint en 2 jours, 4 ou 5 taffes et ca suffit largement, degueulasse, effet trop prononce limite hallus... Beurk ! J'aime pas ca du tout. | » |
| -(Source, Drugstore Cowboy, Psychoactif) |
Aspects légaux
En France, depuis le 27 février 2009, sont classés comme stupéfiants[19] :
- le JWH-018
- le CP 47,497 et ses analogues en C6 (CP 47,497-C6), C8 (CP 47,497-C8) et C9 (CP 47,497-C9)
- le HU-210
Dosages
Les dosages diffèrent d’un composé à l’autre, il convient donc de se renseigner sur les dosages en amont de la consommation. De plus, en raison de la grande puissance de certains cannabinoïdes synthétiques, la quantité de poudre nécessaire peut être extrêmement faible, de l'ordre de quelques milligrammes.
Risques associés
Peu d’études sont disponibles sur les CS, leur toxicité est donc mal connue.
Il semblerait que les CS exposent les usagers à des effets indésirables comparables à ceux du cannabis. Néanmoins, la forte affinité de certains composés (supérieure à celle du THC) pour les récepteurs CB1 laisse supposer que la gravité d’une intoxication aigue pourrait être supérieure[20].
D’autre part, comme précisé dans la section Pharmacologie, les CS n’ont pas tous la même sélectivité vis-à-vis des récepteurs CB1 et CB2. Par conséquent, les profils d’activité ne sont pas nécessairement les mêmes, et le parallèle avec le cannabis trouve ici sa limite.
Chez des consommateurs de CS, ont été rapportés :
- des troubles psychiatriques de type attaques de paniques[20] ou épisodes psychotiques[21] ,
- des convulsions[22] ,
- des troubles cardiovasculaires[23] ,
- des cas d’insuffisances rénales aiguës auraient également été associés à une consommation de CS parmi lesquels le XLR-11 (ou 5F-UR-144) [24]
Plusieurs décès ont également été rapportés suite à l’usage de CS : un consécutif à une crise cardiaque, l’autre par suicide lors d’une attaque de panique[4].
Réduction des Risques
- Se renseigner sur les produits, les effets, les doses et les voies d’administration avant toute prise
- Éviter de consommer en cas de mauvaise tolérance au cannabis
- Privilégier les produits sur lesquels on a le plus de recul
- Ne pas consommer seul
- Commencer à faible dose
- Doser le produit avec une méthode précise, éviter tout dosage « à l’œil »
- Ne pas prendre le volant après avoir consommé
Références
- ↑ 1,0 et 1,1 EMCDDA (OEDT). Drug profile: Cannabinoïdes synthétiques et “Spice.”
- ↑ EMCDDA : Synthetic cannabinoids in Europe
- ↑ 3,0 et 3,1 Wikipedia : Synthetic cannabis
- ↑ 4,0 4,1 4,2 et 4,3 Fattore L, Fratta W. Beyond THC: The New Generation of Cannabinoid Designer Drugs. Front. Behav. Neurosci. 2011;5:60. doi:10.3389/fnbeh.2011.00060.
- ↑ Zuba D, Byrska B, Maciow M. Comparison of “herbal highs” composition. Anal. Bioanal. Chem. 2011;400(1):119–126. doi:10.1007/s00216-011-4743-7.
- ↑ NCSL. Synthetic Cannabinoid Chemical Classes and their Trade Names
- ↑ Wikipedia : Designer drugs
- ↑ PsychoWIKI : Research Chemicals, effets, risques, témoignages
- ↑ Wikipedia : Cannabinoid receptors
- ↑ Lombard C, Nagarkatti M, Nagarkatti P. CB2 cannabinoid receptor agonist, JWH-015 triggers apoptosis in immune cells: Potential role for CB2 selective ligands as immunosuppressive agents. Clin Immunol. 2007;122(3):259–270
- ↑ Xu H, Cheng CL, Chen M, et al. Anti-inflammatory property of the cannabinoid receptor-2-selective agonist JWH-133 in a rodent model of autoimmune uveoretinitis. J Leukoc Biol. 2007;82(3):532–541
- ↑ Tanikawa T, Kurohane K, Imai Y. Regulatory effect of cannabinoid receptor agonist on chemokine-induced lymphocyte chemotaxis. Biol Pharm Bull. 2011;34(7):1090–1093
- ↑ Psychonaut Forum : UR-144 et immunosuppression. Février 2013
- ↑ Johnston, L. D., O‘Malley, P. M., Bachman, J. G., & Schulenberg, J. E. (2013), Monitoring the Future national results on adolescent drug use: Overview of key findings, 2012, Ann Arbor, Institute for Social Research, the University of Michigan, pp. 83.
- ↑ Smith, K. and Flatley, J. (eds) (2011), Drug misuse declared: findings from the 2010/11 British crime survey. England and Wales, Home Office, London.
- ↑ Office for National Statistics (2012), Drug Misuse Declared: Findings from the 2011/12 Crime Survey for England and Wales. Home Office, London.
- ↑ Clinical Committee of the Government Delegation for the National Plan on Drugs (2011), Emerging drugs. Report 6 of the Clinical Committee, Ministry of Health, Madrid.
- ↑ Werse, B., Müller, O., Schell, C., Morgenstern, C. (2011), Jahresbericht MoSyD, Drogentrends in Frankfurt am Main 2010, Centre for Drug Research.
- ↑ Classement comme stupéfiants de substances cannabinoïdes contenues dans le « SPICE »
- ↑ 20,0 et 20,1 UNODC : Synthetic Cannabinoids in Herbal Products.
- ↑ Hurst D, Loeffler G, McLay R. Psychosis Associated With Synthetic Cannabinoid Agonists: A Case Series. Am. J. Psychiatry. 2011;168(10):1119–1119. doi:10.1176/appi.ajp.2011.11010176.
- ↑ Schneir AB, Baumbacher T. Convulsions Associated with the Use of a Synthetic Cannabinoid Product. J. Med. Toxicol. 2012;8(1):62–64. doi:10.1007/s13181-011-0182-2.
- ↑ Mir A, Obafemi A, Young A, Kane C. Myocardial Infarction Associated With Use of the Synthetic Cannabinoid K2. Pediatrics. 2011;128(6):e1622–e1627. doi:10.1542/peds.2010-3823.
- ↑ CDC. Acute Kidney Injury Associated with Synthetic Cannabinoid Use — Multiple States, 2012.