Prévention Grossesse et CBD - effets tératogènes et héréditaires
6589 vues, 15 réponses
1
Les cannabinoïdes retrouvés dans le sang pendant la grossesse ont pour conséquence une raréfaction des neurones dopaminergiques dans le noyau accubens de l'enfant. C'est à dire qu'il sera plus enclin aux addictions d'une part et d'autres parts ils sera difficlement intéressé par les choses de son environnement (la diminution de dopamine étant une conséquence de l'addiction chronique).
Malheureusement je n'ai pas la méta-analyse sous la main pour étayer mon propos mais dans le doute si possible éviter de fumer du cannabis pendant la grossesse (car on le dit pour l'alcool mais pas suffisamment pour le cannabis).
Enfin, on m'a dit à cette conférence que le CBD d'après la littérature scientifique récente était également perturbateur de l'ARN donc une conséquence génétique grave sur la descendance.
Voilà voilà faites attention à vous :)
EDIT : c'est pas ce papier mais c'est mieux que rien, une vieille réf sur l'influence génétique du cannabis :
The genetic epidemiology of cannabis use, abuse and dependence de Arpana Agrawal
Michael T. Lynskey (2006)
https://doi.org/10.1111/j.1360-0443.2006.01399.x
"La consommation maternelle de cannabis diminue les niveaux d'ARNm de DRD2 dans la NAc du fœtus humain"
https://www.sciencedirect.com/science/a … 0672X#sec2
"En conclusion, ces données soulignent le caractère sensible de la période prénatale au cours de laquelle l'exposition au cannabis peut déclencher des modifications épigénétiques qui contribuent aux perturbations à long terme du D2R à l'âge adulte, jetant ainsi les bases d'une vulnérabilité accrue à la toxicomanie et éventuellement à d'autres troubles psychiatriques. les troubles.
Dernière modification par Heashka (27 novembre 2019 à 02:27)
Je cours entre l'hôpital, le laboratoire et les services neuropsychiatriques quand je ne suis pas en conférence à la faculté de médecine pour écouter l'actualité sur l'addictologie.
Hors ligne

- prescripteur
- Adhérent PsychoACTIF
- Inscrit le 22 Feb 2008
- 12631 messages
- Blogs
https://norml.org/news/2017/06/01/study … evelopment
https://www.sciencedirect.com/science/a … 3517301755
les autres
https://www.ncbi.nlm.nih.gov/pubmed/28528172
https://www.ncbi.nlm.nih.gov/pubmed/31619494
https://pediatrics.aappublications.org/ … /e20181889
https://www.ncbi.nlm.nih.gov/pmc/articl … 322776.pdf
https://www.ncbi.nlm.nih.gov/pubmed/21820648
https://www.ncbi.nlm.nih.gov/pmc/articl … 311742.pdf
Mais ne pas oublier tabac et grossesse, notamment
https://www.ncbi.nlm.nih.gov/pubmed/29294364
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6002605/
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3262676/
https://www.ncbi.nlm.nih.gov/pubmed/28957474
Amicalement
Dernière modification par prescripteur (28 novembre 2019 à 14:17)
S'il n'y a pas de solution, il n'y a pas de problème. Devise Shadok (et stoicienne)
Hors ligne
Hors ligne

- Rosetemple
- Drogologue

- Inscrit le 18 May 2019
- 157 messages
- Blogs
Heashka a écrit
"En conclusion, ces données soulignent le caractère sensible de la période prénatale au cours de laquelle l'exposition au cannabis peut déclencher des modifications épigénétiques qui contribuent aux perturbations à long terme du D2R à l'âge adulte, jetant ainsi les bases d'une vulnérabilité accrue à la toxicomanie et éventuellement à d'autres troubles psychiatriques.
Peux-tu étayer ou expliquer ça s'il te plait ? Qu'est-ce que le D2R et en quoi est-ce lié à une vulnérabilité à la "toxicomanie"?
Dédicace à mon amie T'Etoile, la plus gentille et mignonne des personnages magiques !
Hors ligne

- prescripteur
- Adhérent PsychoACTIF
- Inscrit le 22 Feb 2008
- 12631 messages
- Blogs
Le probleme de ces affirmations, c'est qu'on ne sait pas si c'est doses dépendant, si c'est pour une consommations régulière ou pas. Ca fait des affirmations gratuites qui n'avance pas à grand chose au final.
C'est sûr que les études sont difficiles à mener. D'abord parce qu'il est évident qu'on ne peut pas mesurer précisément la consommation qui est largement décrite par l'usagère elle même, avec des biais, surtout pour une substance qui reste illégale au niveau fédéral. Donc dans la plupart des articles on ne note que la consommation de cannabis (oui ou non) et pas la dose ou la fréquence.
Ensuite parce qu'il y a souvent co-consommation, ne serait ce que de tabac. Donc là encore des biais possibles.
Mais je pense que les mères ou futures mères peuvent lire l'état actuel des connaissances pour décider pour elles mêmes.
Amicalement
S'il n'y a pas de solution, il n'y a pas de problème. Devise Shadok (et stoicienne)
Hors ligne

- prescripteur
- Adhérent PsychoACTIF
- Inscrit le 22 Feb 2008
- 12631 messages
- Blogs
Amicalement
Maternal smoking during pregnancy and academic achievement of offspring over time: A registry data-based cohort study
Tabagisme maternel pendant la grossesse et réussite scolaire de la progéniture au fil du temps: étude de cohorte basée sur des données de registre
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6002605/
Résumé
Peu d'études ont évalué l'impact cumulatif du tabagisme chez la mère pendant la grossesse (MSDP) sur les résultats scolaires au fil du temps. Nous avons examiné les relations entre le PDSM et les résultats scolaires des 4e, 7e et 10e années en utilisant les données du registre recueillies à la naissance, pendant la période néonatale et à chaque niveau de la cohorte de naissance de l’étude LIFECOURSE 2000 à Reykjavik, en Islande (N = 1151 , filles = 49,3%). La modélisation de la croissance latente a montré que le MSDP influençait les scores de réussite islandais, standardisés dans une plage allant de 0 à 60, au départ (? = ?0,04) et dans le temps (? = ?0,05). De même, le MSDP était négativement associé à des scores normalisés en mathématiques au départ (ß = ?0,09) et continuait d'exercer un impact négatif sur les scores en mathématiques au fil du temps (ß = ?0,08) après avoir contrôlé le sexe, le revenu, la cohabitation et les mathématiques de base et islandaises. scores de réalisation. Les résultats démontrent l’impact négatif persistant du PDSM sur les résultats scolaires des enfants. Les résultats corroborent l'hypothèse selon laquelle les enfants dont la mère fume au cours du premier trimestre de la grossesse courent en moyenne un risque plus élevé d'obtenir de mauvais résultats scolaires au fil du temps que les enfants dont la mère ne fume pas au cours du premier trimestre. À notre connaissance, il s'agit de la première étude utilisant une conception de cohorte longitudinale pour déterminer si les effets du tabagisme maternel pendant la grossesse pourraient persister dans le temps. Cette étude contribue à l'état actuel des connaissances en fournissant une évaluation axée sur l'impact du tabagisme pendant la grossesse sur les résultats scolaires de l'enfance au début de l'adolescence.
1. Introduction
Il a été démontré que le tabagisme maternel pendant la grossesse (PDSM) avait une relation négative avec le développement physique de la progéniture, aussi bien au stade fœtal qu'au nouveau-né, avec un impact correspondant sur la petite enfance, l'adolescence et même le début de la vie adulte (Clifford et al., 2012; Gilman et al., 2012). , 2008; Inamdar et al., 2015; Ion et al., 2015; Ko et al., 2014; Lanting et al., 2009; Polanska et al., 2015; Roelands et al., 2009; Rogers, 2009). Parmi les complications développementales antepartum et postpartum associées au MSDP figurent l'avortement spontané (Pineles et al., 2014), la grossesse extra-utérine (Roelands et al., 2009), la pré-éclampsie (Roelands et al., 2009; Wikström et al., 2010). ), rupture placentaire (Jauniaux et Burton, 2007), restriction de croissance fœtale, naissance prématurée et faible poids à la naissance (Ko et al., 2014). Le MSDP a également été associé à des dysfonctionnements neurologiques et cognitifs tels que des obstacles au développement du cerveau chez les nourrissons (Wehby et al., 2011), une intégration médiocre visuelle et motrice et une compétence verbale chez les jeunes enfants (Heinonen et al., 2011), un QI inférieur, diminution des résultats scolaires et déficiences intellectuelles chez les enfants des écoles primaires (Alloway et Alloway, 2010; Cornelius et al., 2012; Duckworth et Seligman, 2005; Kafouri et al., 2009; Pineles et al., 2014; Braun et al., 2014). 2009; Gilman et al., 2008; Huijbregts et al., 2006), ainsi que des problèmes de comportement tels que les troubles de la conduite et les troubles de l'hyperactivité avec déficit de l'attention (THADA) chez les enfants âgés de 6 à 16 ans (Gaysina et al., 2013; Langley et al., 2007).
Plusieurs études ont mis en évidence une réduction des résultats scolaires chez la progéniture des mères qui fumaient du tabac pendant la grossesse (Lambe et al., 2006; Martin et al., 2006; O'Callaghan et al., 2010). Par exemple, Lambe et al. (2006) ont examiné plus de 400 000 élèves suédois âgés de 15 ans et leur performance scolaire mesurée à l'aide de scores sommaires obtenus sur 16 notes en fonction de l'exposition prénatale à la fumée de cigarette. Les résultats ont montré un déficit chez les personnes exposées à la fumée de cigarette prénatale. Une étude finlandaise a évalué les notes scolaires moyennes pour toutes les matières chez les enfants de 12 ans et a mis en évidence une réduction des résultats scolaires chez les enfants de fumeurs par rapport aux non-fumeurs (Martin et al., 2006). Des résultats similaires ont également été rapportés dans une étude prospective australienne portant sur plus de 7 000 mères et leurs enfants (O'Callaghan et al., 2010). À l'inverse, les données du projet national de collaboration des États-Unis, qui comprenait un échantillon d'environ 50 000 participants, n'ont révélé aucune association entre le MSDP et les résultats scolaires, mesurée à l'aide de scores standardisés en lecture, orthographe et calcul (Gilman et al., 2008). Ce résultat concordait avec une étude suédoise quasi expérimentale utilisant une approche de comparaison entre frères et sœurs parmi des élèves de 15 ans; il n'y avait pas de différences dans les notes scolaires et les compétences en mathématiques parmi les frères et sœurs exposés et non exposés (D'Onofrio et al., 2010).
En plus de l’incohérence des connaissances actuelles concernant les relations entre le MSDP et les résultats scolaires de la progéniture, peu d’études ont cherché à évaluer l’impact du MSDP sur les résultats scolaires à plusieurs moments, malgré la nécessité et la nécessité de telles études (Martin et al ., 2006). Les quelques études qui ont inclus une évaluation des résultats académiques à plus d'une période n'ont pas utilisé de modèles statistiques qui tiennent compte de la structure temporelle liée dans les données et donc du potentiel d'un effet cumulatif dans le temps. Par exemple, Gilman et al. (2008) ont évalué les relations entre l'exposition prénatale à la fumée et les résultats scolaires chez les enfants de 4 et 7 ans respectivement, mais n'ont trouvé aucune association après contrôle des facteurs de confusion potentiels, et Kristjansson et al. (2017) ont trouvé des relations négatives entre le PDSM et les résultats scolaires des enfants âgés de 10, 13 et 15 ans. Ainsi, pour comprendre l'impact cumulatif à long terme du PDSM sur les résultats scolaires, les études doivent utiliser des mesures cohérentes réalisation sur plusieurs périodes de développement, et des méthodes analytiques qui les teste simultanément dans un modèle cohérent.
Un autre problème lié aux évaluations précédentes a été la variation des covariables étudiées. Ceux-ci incluent à la fois des facteurs liés à la naissance, tels que le poids à la naissance et les caractéristiques familiales, susceptibles de contribuer à la relation entre le PDSM et les résultats cognitifs (Gilman et al., 2008; Lawlor et al., 2006). des facteurs tels que l'éducation de la mère sont plus susceptibles que les mesures liées à la naissance d'expliquer les résultats cognitifs (Batty et al., 2006; Breslau et al., 2005; Clifford et al., 2012; Wehby et al., 2011). Dans le même temps, quelques études ont inclus un large éventail de résultats liés à la naissance, mais ont omis les facteurs familiaux et sociaux au moment de l'évaluation (Lambe et al., 2006), et d'autres ont inclus les caractéristiques sociales et familiales au moment de l'évaluation. d'évaluation mais n'ont pas inclus les facteurs liés à la naissance. Compte tenu de l'importance relative de ces deux ensembles de covariables et d'une plus grande cohérence dans le choix des covariables (Clifford et al., 2012; Inamdar et al., 2015; Ion et al., 2015; Ko et al., 2014; Lanting et al., 2009; Roelands et al., 2009), des études qui intègrent les deux tout en contrôlant simultanément les facteurs sociaux et familiaux à différentes périodes d'évaluation pourraient mieux éclairer la relation entre le PDSM et les résultats scolaires.
Le but de cette étude était d’améliorer la compréhension actuelle de l’impact potentiel à long terme du PDSM sur les résultats scolaires. Nous avons examiné l’impact du MSDP sur les résultats scolaires normalisés à l’âge de 10 à 11 ans (4e année), 13 à 14 ans (7e année) et 15 à 16 ans (10e année). Les données ont été recueillies à la naissance, pendant la période néonatale, et à chaque niveau. Nous émettons l'hypothèse que le tabagisme maternel conduirait à la fois à des scores de réalisation plus bas et à des scores cumulés plus faibles au fil du temps.
2. Méthodes
2.1. Échantillon et participants
Ce rapport est basé sur les données de l'étude LIFECOURSE sur les facteurs de risque et de protection menée par le Centre de recherche et d'analyse sociales (ICSRA) de l'Université de Reykjavik en Islande. LIFECOURSE est une étude de cohorte sur le développement qui couvre les premières années de la vie d'une cohorte de naissance d'enfants de la naissance à 15/16 ans. Le cadre théorique de l'étude a été décrit ailleurs (Sigfusdottir et al., 2017). La base de sondage de l'étude comprend tous les enfants nés et résidant à Reykjavik, en Islande, en 2000 (N = 1151, filles = 49,3%). Le matériel de l’étude pour l’enquête comprenait une combinaison de données du registre officiel de plusieurs banques de données nationales assemblées de 2014 à 2016. Pour les besoins de la présente analyse, nous avons utilisé des données de registre rétrospectives provenant des sources suivantes: i) Registre national des naissances de l’Université Landspitali Hôpital, ii) dossiers prénatals du registre des soins maternels des cliniques de soins de santé primaires, tous deux supervisés par la Direction islandaise de la santé, qui supervise l’ensemble du système de registres de santé en Islande, iii) de l’Institut de test pédagogique, supervisé par le ministère de la Santé. Education, Science et Culture, et iv) le Bureau de statistique d'Islande. L'étude a été examinée et approuvée par le Comité national de bioéthique d'Islande (ce qui équivaut à une IRB nationale) et l'étude a été enregistrée et reconnue par l'autorité de protection des personnes.
2.2. Les mesures
2.2.1. Réussite
Les données sur les scores de réussite en mathématiques et en islandais des 4ème (10-11 ans), 7ème (13-14 ans) et 10ème (15-16 ans) provenaient de la base de données ETI. La notation en Islande est donnée sur une échelle numérique allant de 0 à 10, 5 étant «satisfaisant» et supérieur à 5 et supérieure ou égale à 7,25 considérée comme une note de première classe. Aux fins de cette évaluation, l'ETI a attribué des notes standardisées sur une échelle de 0 à 60 pour chaque matière, avec des scores moyens fixés à 30 et une échelle combinée pour les deux matières allant de 0 à 120.
2.2.2. Revenu annuel des ménages
Les données sur le revenu total du ménage étaient disponibles par année et calculées dans l'enquête comme la combinaison additive du revenu de l'emploi, du capital et de tout autre revenu. Une analyse exploratoire des données de toutes les années a révélé que la dernière année de revenu disponible, 2013, avait la relation statistique la plus forte avec les variables de réalisation. Cette variable, allant de 0 à 172 millions d’ISK, a ensuite été divisée en déciles, avec 10% dans chaque groupe, afin de tenir compte des excès de 0 et d’un très fort biais positif.
2.2.3. Tabagisme maternel
Le tabagisme maternel pendant la grossesse a été évalué lors de la première visite prénatale qui a généralement lieu vers la fin du premier trimestre en Islande. On a demandé aux femmes enceintes si elles fumaient du tabac ou si elles le faisaient avant de savoir si elles deviendraient enceintes. Le statut de fumeur était initialement codé comme (0) non, (1) oui, parfois pendant la grossesse, et (2) oui, avant de connaître la grossesse. Des travaux antérieurs (Kristjansson et al., 2017) ont démontré que ceux qui ont approuvé la dernière option (10% de la population) étaient plus similaires à ceux qui ont dit non que les fumeurs réguliers de cigarettes. Ainsi, nous avons recodé cette variable dans (1) oui, parfois pendant la grossesse et (0) non-fumeur ou tabagisme avant d’être informé de la grossesse.
2.2.4. La cohabitation à la naissance
La cohabitation maternelle avec le père au moment de la naissance provient de la base de données du registre des naissances et a été recodée dans (1) oui, (0) non.
2.2.5. Sexe de l'enfant
Les données sur le sexe à la naissance proviennent de la base de données du registre des naissances et ont été recodées en (1) homme, (0) femme.
.3. Procédure
Les informations de contact pour l'échantillon ont été obtenues auprès du Bureau national de la statistique et des agences sœurs. Un numéro d'identification de recherche non traçable a été créé pour chaque participant et des clés USB contenant ces informations ont été transmises au personnel local de chaque site avec l'autorité appropriée pour traiter les informations sensibles et personnelles. Les données collectées ont ensuite été préparées et transférées dans des fichiers sur chaque site au cours de la période 2014-2016 en utilisant le numéro d'identification de la recherche pour identifier les participants tout en supprimant toutes les informations personnelles lors de la livraison des fichiers à l'équipe de recherche. Les données disponibles pour chaque variable du registre sont comprises entre 980 et 1149, soit entre 85,1% et 99,8% de l'échantillon de l'étude. Une clé reliant des noms de personne et des informations de contact à des identifiants de recherche est gérée par une tierce partie dans les cliniques de soins de santé primaires et n'est pas accessible à l'équipe de recherche.
2.4. analyses statistiques
Toutes les analyses ont été menées dans SAS v. 9.4 (SAS, 2017). Des statistiques descriptives ont été générées pour toutes les variables incluses dans l’analyse, à savoir la fréquence et le pourcentage valide de déclaration pour les variables catégorielles ou binaires, ainsi que la moyenne, l’écart type et les valeurs minimale et maximale pour les variables continues. Les corrélations tau de Pearson, Point-Biserial et Kendall ont été calculées pour toutes les variables de l'étude en fonction du type de variable. Des tests t d'échantillons indépendants supplémentaires, avec une valeur alpha de 0,05, ont été inclus pour les différences de test entre chaque mesure de rendement et le statut tabagique de la mère.
Pour tester la question clé de la recherche concernant l’impact du tabagisme chez les mères sur les résultats obtenus au fil du temps, nous avons suivi une approche analytique fondée sur un modèle de croissance latente, qui utilisait une modélisation par équation structurelle permettant des mesures répétées au fil du temps via des intersections et des pentes latentes. Cette technique analytique présente des avantages par rapport aux méthodes plus traditionnelles d’analyse de mesures répétées en abordant les différences individuelles dans les trajectoires de croissance en termes de variables latentes (c’est-à-dire en permettant aux variables latentes de représenter les intersections et les pentes dans le temps; Curran et Muthen, 1999; McArdle, 1988). Dans ce modèle, l'estimation du paramètre d'interception est interprétée comme la courbe de croissance prévue lorsque l'ensemble des prédicteurs sont tous égaux à 0 (c'est-à-dire au niveau de référence) et l'estimation du paramètre de pente est interprétée comme la courbe de croissance prévue pour chaque changement d'unité dans le temps. .
Une série de modèles a été réalisée suivant l'approche recommandée par Tan et al. (2010) et modifié selon les besoins pour les mises à jour dans la procédure SAS PROC CALIS. Cette approche comprenait l’estimation du maximum de vraisemblance, l’essai des composants de mesure liés aux mesures répétées (croissance linéaire et non linéaire, régression automatique et moyenne mobile, ARMA), d’abord sur chaque ensemble individuel de mesures de rendement, puis sur la combinaison des résultats. mesures, y compris les variables multivariées, associatives, les facteurs de courbes, les facteurs de courbes conditionnels et les facteurs de courbes ARMA associés, LGM.
Des tests de mesure supplémentaires ont inclus des pentes et des intersections communes entre les modèles de mesure et une évaluation des erreurs corrélées. Les modèles ont été comparés à diverses mesures de qualité d'ajustement, notamment les critères d'information d'Akaike (AIC) privilégiés parmi les plus bas d'un modèle à l'autre, le khi-carré non significatif du modèle (P> 0,05), l'indice comparatif d'ajustement (CFI)> 0,95 et la valeur moyenne Erreur carrée d'approximation (RMSEA) <0,05 ou 90% d'intervalle de confiance, y compris 0,05. Une fois que le modèle de mesure le mieux adapté a été déterminé, les composants structurels ont été inclus dans le modèle, comme suggéré par la pertinence du modèle théorique et l'ajustement statistique.
Des tests supplémentaires ont été réalisés en évaluant un modèle sans sexe contre; 1) un modèle avec le genre en tant que covariable et, 2) le sexe en tant que variable de stratification pour les différences fondées sur les groupes. Un modèle basé sur le groupe (stratification par sexe) a produit l’ajustement le plus pauvre. Les modèles les mieux adaptés sont présentés avec et sans sexe comme covariables, tout en testant le modèle imbriqué pour les différences khi-deux où l'ajustement amélioré pour un modèle plus complexe a été déterminé comme un test de différence significative (p <0,05). Les estimations de paramètres, y compris les coefficients bêta normalisés et non normalisés avec les valeurs t, sont présentées pour les modèles structurels.
3. Résultats
3.1. Statistiques descriptives
Le tableau 1 présente les corrélations pour toutes les variables de l'étude. Environ un quart de l'échantillon (19%) a déclaré avoir fumé pendant la grossesse, mais des corrélations négatives significatives ont été observées entre le tabagisme maternel et toutes les variables de l'étude, à l'exception du sexe masculin. Des tests t indépendants ont montré des différences significatives (toutes p <0,01) en mathématiques, ceux qui ont déclaré que le tabagisme maternel avait des moyennes plus faibles par rapport à l'absence de tabagisme maternel en 4e année: 27,69 (9,81) contre 31,52 (10,37), 7e année: 27.69 (9.91) v. 31.66 (9.98) et 10e année: 28.06 (10.52) v. 32.48 (10.11). Des différences ont également été observées, bien que moins marquées, dans les scores d’acquisition du islandais, notamment en 4e année: 29,75 (10,16) v. 32,16 (10,30), P = 0,01, 7e année: 28,99 (10,73) v. 31,90 (10,12), P = 0,01 et 10e année: 29,03 (10,28) v. 32,58 (10,57), p <0,01.3.2. Modèles de croissance latents
Le modèle de mesure le mieux adapté était un modèle LGM associatif avec des erreurs corrélées entre les mathématiques et les notes islandaises en 4e année, en 7e année et en 10e année. Les ajouts structurels les mieux adaptés incluaient notamment la possibilité de créer une structure croisée entre les intersections sur les pentes, ce qui permet de corréler les perturbations entre les pentes et les intersections et les covariables qui ont impacté de manière sélective les intersections et les pentes pour les résultats en mathématiques et en islandais. Le tableau 2 montre l'ajustement du modèle et les comparaisons du modèle final en excluant le genre en tant que covariable, le genre en tant que covariable et une stratification par genre. Le test de différence du khi-deux suggère que les deux modèles s’adaptent bien (p = 0,11) et que l’inclusion du sexe en tant que covariable ne nuit donc pas à notre ajustement. Un excellent ajustement du modèle a été obtenu pour le modèle final. Le tableau 3 donne les estimations de paramètres pour le modèle, y compris le genre en tant que covariable. Notamment, le tabagisme maternel est négativement associé aux scores de base en mathématiques (ß = ?0,09) après contrôle du sexe et du revenu. Il existe des preuves statistiques modérées selon lesquelles il continue d’avoir une incidence négative sur les notes obtenues en mathématiques au fil du temps (? = ?0,08) après contrôle des résultats en termes de sexe, de revenu, de cohabitation, et en mathématiques et en islandais. De même, le tabagisme maternel influence moins fortement les résultats scolaires islandais de base (? = ?0,04) que les résultats islandais dans le temps (? = ?0,05).
4. Discussion
Le PDSM a un impact négatif important, et pertinent sur le plan pédagogique, sur la situation de référence en mathématiques et en scores de réalisation en islandais, et continue à avoir un impact négatif sur ces scores au fil du temps. Les relations bi-variées ont révélé que le sexe masculin n'était pas associé au MSDP; Le sexe de l'enfant peut jouer le rôle de modérateur dans la relation entre le PDSM et la réussite scolaire. Nous avons donc inclus un modèle avec et sans genre comme covariable. Comme prévu, des tests d'échantillons indépendants ont montré que les enfants de ceux qui avaient déclaré fumer au cours du premier trimestre de la grossesse avaient des scores moyens inférieurs pour les deux matières (mathématiques et islandais) aux 4e, 7e et 10e années par rapport à ceux dont la mère n'a pas fumé pendant le premier trimestre de la grossesse.
Nous avons étendu notre approche analytique avec LGM, avec et sans sexe en tant que médiateur. Les modèles LGM ont également démontré l’impact négatif du MSDP sur les résultats scolaires, tant en mathématiques qu'en résultats islandais. Plus spécifiquement, le tabagisme maternel était prédictif d'une réduction des scores en mathématiques au départ et dans le temps, sans distinction de sexe. Des résultats similaires ont été observés pour les scores de réussite islandais au départ et dans le temps, bien que l'ampleur des effets n'ait pas été aussi grande que les scores en mathématiques. Ces résultats suggèrent que les effets négatifs de l'exposition prénatale au tabagisme maternel pourraient affecter négativement les capacités cognitives de la progéniture et, peut-être plus profondément, que cet effet négatif pourrait persister dans le temps.
Il existe plusieurs explications plausibles à ces résultats. Premièrement, le monoxyde de carbone contenu dans la fumée de cigarette absorbée par la mère et le fœtus crée des niveaux élevés de carboxyhémoglobine; cela réduit le flux sanguin oxygéné intra-utérin et peut entraîner une hypoxie fœtale, une restriction de croissance intra-utérine et un faible poids à la naissance (Liu et al., 2007; Mezzacappa et al., 2011; Rogers, 2009; Soothill et al., 1996). Deuxièmement, la nicotine a été identifiée comme un neurotératogène qui modifie les voies de développement neurales du cerveau et peut réduire la croissance du cerveau et le périmètre crânien (Dwyer et al., 2009; Pauly et Slotkin, 2008; Roza et al., 2007). Un tour de tête réduit chez les nourrissons de faible poids à la naissance est associé à une réduction des capacités cognitives et neuropsychologiques chez les enfants d'âge scolaire (Lundberg et al., 2010). L'exposition prénatale à la nicotine a également été associée à des anomalies neurocomportementales postnatales telles que le trouble du déficit de l'attention, des troubles d'apprentissage, l'hyperactivité et un risque accru de problèmes de comportement (Lundberg et al., 2010; Pauly et Slotkin, 2008; Peterson et al., 2008). , 2006; Rogers, 2009; Roza et al., 2007).
Les preuves de cette étude sont cohérentes avec les recherches précédentes, qui avaient identifié une réduction des résultats scolaires chez les enfants exposés au tabagisme maternel pendant la grossesse (Lambe et al., 2006; Martin et al., 2006; O'Callaghan et al., 2002). 2010). Des études antérieures examinant la relation entre le PDSM et les résultats scolaires corrigée pour tenir compte des caractéristiques liées à la naissance (Lambe et al., 2006) ou familiales (O'Callaghan et al., 2010), limitant ainsi l'impact de facteurs de confusion potentiels; cependant, les résultats scolaires n'ont pas été évalués à différents moments. Par conséquent, la présente étude cherchait à utiliser une évaluation longitudinale permettant d'identifier les changements possibles dans l'association entre le PDSM et les résultats scolaires au fil du temps. En revanche, cette étude est en contradiction avec les études de Gilman et al. (2008) et D'Onofrio et al. (2010); leurs résultats n'ont montré aucune association avec le MSDP et les résultats scolaires. Une revue de Clifford et al. (2012) ont également identifié des relations nulles similaires, ou légères, qui ont ensuite été atténuées par d'autres facteurs.
Cette étude présente plusieurs points forts notables. Premièrement, nous avons utilisé un modèle de cohorte longitudinale qui permettait des évaluations à trois moments différents. À notre connaissance, il s'agit de la première étude à utiliser une telle conception pour évaluer la relation entre le PDSM et les résultats scolaires. Deuxièmement, l'utilisation des données du registre est plus susceptible de contourner les erreurs aléatoires associées à l'autodéclaration et renforce ainsi la validité de nos résultats. Troisièmement, l'utilisation d'une approche analytique qui prend en compte la corrélation des données ajoute de la robustesse à la méthodologie et aux résultats. Malgré ces atouts, cette étude n’est pas sans limites. Premièrement, il n'existait aucune donnée permettant de vérifier le statut tabagique des mères ou de déterminer la durée ou la fréquence du tabagisme au-delà du premier trimestre de la grossesse. Deuxièmement, nous n'avons pas été en mesure de collecter des données concernant l'exposition au tabagisme passif provenant, par exemple, d'un partenaire fumeur ou d'un autre membre de la famille. En outre, les résultats neurodéveloppementaux peuvent être partiellement influencés par les gènes et l'éducation maternelle (Huijbregts et al., 2006; Skoglund et al., 2014); Cependant, nous n'avons pas pu obtenir de données sur les niveaux d'éducation des parents ni sur le patrimoine génétique. Enfin, le QI maternel, la qualité de l’environnement familial,
5. Conclusions
Le tabagisme maternel pendant la grossesse a un impact négatif sur les résultats scolaires dès l'enfance et jusqu'au début de l'adolescence. Ces effets négatifs persistent quels que soient le sexe et le temps. Fumer au cours du premier trimestre de la grossesse peut avoir un impact négatif durable sur le potentiel académique de la progéniture. Les recherches futures devraient chercher à reproduire ces résultats auprès de populations plus diverses, tout en contrôlant les niveaux d'éducation de la mère et l'exposition cumulée au tabagisme tout au long de la grossesse.
S'il n'y a pas de solution, il n'y a pas de problème. Devise Shadok (et stoicienne)
Hors ligne
prescripteur a écrit
prescripteur
Salut Doc,
C est pas très surprenant comme résultat d étude mais de le voir de manière aussi précise ça fais quand même bien mal au c**.
Merci d avoir partager en tout, très intéressant.
A plus,
Ocram
Hors ligne

- prescripteur
- Adhérent PsychoACTIF
- Inscrit le 22 Feb 2008
- 12631 messages
- Blogs
les numeros de bibliographie ne sont pas retirés. Si vous voulez voir les refs il faut aller sur l'adresse de l'article en anglais.
https://pediatrics.aappublications.org/ … /e20181889
Mais il me parait important aussi de lire
https://www.ncbi.nlm.nih.gov/pubmed/28528172
Cannabis and pregnancy: Maternal child health implications during a period of drug policy liberalization.
La consommation de cannabis est courante et augmente chez les femmes aux États-Unis. Les politiques des États évoluent avec un mouvement de décriminalisation et de légalisation. Nous explorons les implications de la libéralisation du cannabis pour la santé maternelle et infantile. La plupart des femmes qui utilisent du cannabis ont arrêté ou réduit leur consommation au cours de la grossesse. Bien que les femmes s'inquiètent des effets possibles du cannabis sur la santé, les prestataires de services de conseil font un travail médiocre. Il est théoriquement possible que le cannabis interfère avec le neurodéveloppement, mais les données humaines n’ont pas mis en évidence de différence significative à long terme entre les enfants exposés in utero au cannabis et ceux qui ne le sont pas. Une diffusion scientifiquement exacte des données sur les effets du cannabis est nécessaire. Les risques ne doivent être ni surestimés ni minimisés, et le statut juridique d'une substance ne doit pas être assimilé à de la sécurité. La diminution ou l'arrêt de l'utilisation de toutes les drogues à usage récréatif devrait être encouragée pendant la grossesse. Les prestataires doivent reconnaître que même dans les environnements où le cannabis est légal, les femmes enceintes peuvent être impliquées dans les services de protection de l'enfance. Dans les États où la consommation de substances psychoactives est considérée comme un abus envers les enfants, cela peut être particulièrement catastrophique. Surtout, les soins aux femmes enceintes qui utilisent du cannabis devraient être non punitifs et fondés sur le respect de l'autonomie de la patiente.
nb= c'est moi qui ai mis en gras
Amicalement
Marijuana Use During Pregnancy and Breastfeeding: Implications for Neonatal and Childhood Outcomes
Consommation de marijuana durant la grossesse et l'allaitement: conséquences pour les suivis néonatals et infantiles
https://pediatrics.aappublications.org/ … /e20181889
Résumé
La marijuana est l'une des substances les plus largement utilisées pendant la grossesse aux États-Unis. De nouvelles données sur la capacité des cannabinoïdes de traverser le placenta et d’affecter le développement du fœtus suscitent des inquiétudes quant à l’issue de la grossesse et aux conséquences à long terme pour le nourrisson ou l’enfant. Les médias sociaux sont utilisés pour vanter l'utilisation de la marijuana pour les nausées sévères associées à la grossesse. Des préoccupations ont également été exprimées au sujet de la consommation de marijuana par les mères qui allaitent.
Avec ce rapport clinique, nous fournissons des données sur les taux actuels de consommation de marijuana chez les femmes enceintes et allaitantes, discutons des connaissances sur les effets de la marijuana sur le développement du fœtus et sur les conséquences neurodéveloppementales et comportementales ultérieures, ainsi que sur les implications pour l’éducation et les politiques.
Grossesse et consommation de marijuana
Épidémiologie
Les données de 2016 rapportées dans l'Enquête nationale sur la consommation de drogues et la santé (NSDUH) ont révélé que 4,9% des femmes enceintes âgées de 15 à 44 ans avaient déclaré avoir consommé de la marijuana le mois dernier, contre 11% des femmes non enceintes du même âge. groupe.1
Il s’agit d’une augmentation par rapport à l’année précédente de 3,4% et 10,3%, respectivement. Parmi les femmes enceintes âgées de 18 à 25 ans, 8,5% ont déclaré avoir consommé de la marijuana au cours du dernier mois en 2016, comparativement à 3,3% des femmes enceintes âgées de 26 à 44 ans. Bien que les données de 2016 ne soient pas disponibles pour les femmes enceintes de 15 à 17 ans, les données de 2012-2013 ont révélé que 14,6% avaient déclaré avoir consommé des drogues illicites † au cours du dernier mois. Parmi ces substances illicites, la marijuana est la substance la plus couramment utilisée par les femmes enceintes. Des taux très variables sont rapportés parmi les études publiées aux États-Unis et au Royaume-Uni.
En 2001, les auteurs d’une étude multicentrique sur le mode de vie aux États-Unis ont signalé une prévalence de 7,2% du ?-9-tétrahydrocannabinol (THC), substance psychoactive présente dans la marijuana, dans des échantillons de méconium pour nourrissons .2
Les auteurs d’une étude pilote menée en 2006 au Royaume-Uni 13,25% d'une cohorte de nouveau-nés écossais avaient des échantillons de méconium dont les résultats étaient positifs pour le tétrahydrocannabinol et / ou le tétrahydrocannabinol-acide 9-carboxylique.3 Les taux d'utilisation de la marijuana dans les villes, observés entre 15 et 15 % et 28% 4–6 À partir des données de la NSDUH de 2002 à 2014, Brown et al7 ont signalé que la prévalence de la consommation de marijuana au cours du mois précédent chez les femmes enceintes de 18 à 44 ans a augmenté de 2,37% à 3,84%. taux d'utilisation rapportés chez les femmes âgées de 18 à 25 ans (7,47% en 2014). Plusieurs enquêtes spécifiques à des États ont également été utilisées pour documenter les taux croissants de consommation de marijuana chez les femmes enceintes. Le Système de surveillance de l’évaluation du risque de grossesse (PRAMS), un projet de surveillance des centres de contrôle et de prévention des maladies et des services de santé d’Etat, recueille des données spécifiques à l’état et à la population sur les attitudes et expériences maternelles avant, pendant et après la grossesse (disponibles à cdc.gov/prams). PRAMS a mené des enquêtes sur un échantillon de femmes vivant dans le Vermont ayant eu une naissance vivante depuis 2001 et a posé des questions sur la consommation de marijuana pendant la grossesse depuis 2009. 8 En 2013, 9,4% des femmes du Vermont ont déclaré avoir consommé de la marijuana pendant leur grossesse. 2009. Les données PRAMS d'Hawaii ont révélé que les femmes qui déclaraient avoir eu des nausées importantes pendant leur grossesse rapportaient des taux plus élevés de consommation de marijuana (3,7%) par rapport aux femmes enceintes sans nausées (2,3%) 9. Le NSDUH de 2012 a révélé que les femmes enceintes leur consommation de marijuana est passée de 9,0% à 4,8% au premier et au deuxième trimestres, respectivement, à 2,4% au troisième trimestre. Les taux déclarés de consommation de tabac pendant la grossesse ont diminué de 19,9% à 13,4% et à 12,8% aux premier, deuxième et troisième trimestres, respectivement.
Les auteurs d'autres études ont constaté que 48% à 60% des consommateurs de marijuana déclaraient en faire usage pendant toute leur grossesse, estimant qu'il était plus sûr que le tabac4,10,11. Dans l'étude longitudinale sur le développement et la petite enfance du Royaume-Uni, Moore et tous ont constaté que la plupart des femmes enceintes consommant de la cocaïne, de l'ecstasy, de la méthylènedioxyméthamphétamine et d'autres stimulants ont cessé de consommer ces substances dès le deuxième trimestre, mais 48% des utilisateurs précédents de marijuana ont continué à consommer de la marijuana ainsi que de l'alcool (64%) et du tabac (46%). ) tout au long de leur grossesse. En outre, l’étude sur le développement longitudinal et la petite enfance a révélé que la fréquence et les quantités de marijuana et de tabac étaient maintenues tout au long de la grossesse, tout comme les niveaux enregistrés avant la grossesse, alors que la consommation d’alcool signalée était réduite. Les données PRAMS du Vermont ont également révélé que pour les naissances de 2013, 44,6% des femmes qui déclaraient être des fumeurs de marijuana avant leur grossesse continuaient à en consommer pendant la grossesse.8 Contrairement à ces études, Forray et al ont constaté que, sur 101 femmes ayant déclaré en consommer. au début de la grossesse et ayant bénéficié d'un conseil en matière d'abus de substances psychoactives, 78% se sont abstenus 151 jours plus tard en moyenne et jusqu'à l'accouchement.
Dans une étude de cohorte rétrospective portant sur des femmes prénatales et accouchant dans leur établissement, 21,8% des femmes recevant des soins prénatals et accouchant dans leur établissement ont initialement présenté des résultats de dépistage positifs pour la consommation de marijuana (par auto-évaluation ou toxicologie urinaire), dans une étude rétrospective de cohorte13 mais seulement 1,9% avaient des résultats de dépistage de la marijuana positifs au moment de l’accouchement. Ils ont attribué le taux élevé d'abandon de la consommation de marijuana pendant la grossesse à des possibilités d'éducation concernant les effets néfastes de la consommation de drogues, y compris le tabac et la marijuana, lors des visites prénatales13.
La consommation de marijuana pendant la grossesse a été associée à des taux plus élevés de consommation de substances licites et illicites et à certaines caractéristiques socio-économiques et démographiques. Par exemple, dans l’étude PRAMS au Vermont, les chercheurs ont découvert que les femmes enceintes qui déclaraient avoir consommé de la marijuana étaient plus susceptibles d’être plus jeunes (moins de 25 ans), de faire partie de ménages à faible revenu, de fumer des cigarettes et d’avoir déclaré un facteur de stress émotionnel important (traumatique, financier ou lié au partenaire) avant ou pendant la grossesse.8 Mark et al13 ont constaté que la marijuana était plus répandue chez les femmes qui déclaraient être au chômage, sans diplôme d'études secondaires, consommant de l'alcool ou des cigarettes, déprimé ou victime d'abus. Aux Pays-Bas, El Marroun et al14 ont découvert dans un échantillon de plus de 7 000 femmes enceintes que 85% des fumeurs de marijuana fumaient de la cigarette. Schempf et Strobino6 ont constaté que la consommation de marijuana n'était pas liée de manière indépendante aux soins prénatals. Dans la population de femmes urbaines pauvres, le manque de soins prénatals adéquats, défini comme une ou plusieurs visites prénatales, était significativement plus probable parmi les consommateurs de cocaïne et d'opiacés, mais non les consommateurs de marijuana.6 La peur était liée à cette corrélation avec la consommation de cocaïne et d'opiacés d'être signalés à la police ou aux services de protection de l'enfance et réduire les avantages perçus des soins prénatals. Ces études soulignent l’importance de tenir compte de la confusion potentielle de variables démographiques et comportementales supplémentaires lors de l’évaluation du rôle indépendant de la marijuana sur la grossesse et les résultats pour le fœtus et l’enfant.
Il est important de noter que les taux de consommation de marijuana déclarés peuvent varier en fonction de la méthode de dépistage utilisée. Les recommandations actuelles recommandent le dépistage systématique de l’usage de substances chez toutes les femmes enceintes au moyen de questionnaires validés ou de conversations avec les patientes5,17. Les auteurs de la plupart des études à ce jour se sont principalement fiés à l’auto-évaluation, ce qui peut avoir entraîné une sous-estimation significative par rapport aux questionnaires ou aux évaluations. mesures objectives en utilisant des échantillons de dépistage d'urine ou de méconium. Cependant, même ces mesures objectives donneront des résultats variables, en fonction de la chronicité et de l'intensité de l'utilisation, ainsi que de la récurrence de l'utilisation en fonction du moment où un échantillon d'urine est obtenu. Avec le nombre croissant d'États légalisant l'usage de la marijuana et vantant Internet comme un traitement sûr des nausées pendant la grossesse, la consommation actuelle de marijuana est préoccupante. Les prestataires de soins de santé peuvent constater une augmentation du nombre de femmes enceintes consommant de la marijuana pendant au moins une partie de leur grossesse18.
On ne sait pas vraiment pourquoi les femmes enceintes choisissent de consommer de la marijuana pendant leur grossesse, car peu de données sont disponibles sur les avantages de la consommation de marijuana pendant la grossesse. Roberson et ses collaborateurs 9 ont constaté que les femmes qui déclaraient avoir consommé de la marijuana pendant la grossesse étaient plus susceptibles de déclarer avoir eu de graves nausées et vomissements (3,7%) que celles n'ayant pas présenté ces symptômes graves (2,7%). Dans une deuxième étude sur les femmes consommant de la marijuana au cours de leur grossesse, 51% ont déclaré en prendre pour soulager les nausées et les vomissements, et 92% de ces femmes ont signalé son efficacité; aucun témoin n'a été inclus dans cette étude.19 Bien que l'utilisation de la marijuana soit vantée sur les médias sociaux comme un traitement efficace et sûr des nausées et vomissements de grossesse, il n'y a actuellement aucune indication pour son utilisation pendant la grossesse; le Collège américain des obstétriciens et gynécologues (ACOG) l'a clairement indiqué dans l'avis de sa commission en 2015.5 Il convient de noter qu'aucun État ayant des lois légales sur la marijuana à usage médical ne mentionne la grossesse comme une contre-indication à la recommandation ou à la délivrance de marijuana à des fins médicales.
Pharmacocinétique des cannabinoïdes pendant la grossesse
La marijuana peut affecter les fonctions de transport normales et le statut physiologique du placenta tout au long de la grossesse.20 Une étude a révélé qu'une exposition à court terme au cannabidiol, une substance non psychoactive trouvée dans la marijuana, pouvait améliorer la perméabilité de la barrière placentaire aux agents pharmacologiques et aux substances de loisirs. El Marroun et ses collaborateurs22 ont constaté que la consommation de marijuana pendant la grossesse, par rapport à l'absence de marijuana ou au tabac, entraînait une augmentation de l'indice de résistance et de la pulsatilité de l'artère utérine, entraînant effets sur le débit sanguin utérin, tels que l'augmentation de la résistance placentaire et la réduction de la circulation placentaire.
Les études ayant servi à évaluer la capacité des métabolites des drogues, y compris la marijuana, à traverser le placenta ne sont pas récentes et ont révélé que des substances récréatives et licites traversent directement le placenta, soit par diffusion passive, soit, moins fréquemment, par voie active. transport ou pinocytose23. Parmi les nombreux cannabinoïdes présents dans la marijuana, la substance la plus responsable des effets psychoactifs, le THC, traverse facilement le placenta.24 La molécule de THC est hautement lipophile et se distribue rapidement dans le cerveau et la graisse le fœtus après ingestion ou inhalation par la femme enceinte. Après l'ingestion maternelle, les concentrations de THC dans le sang fœtal représentent environ un tiers à un dixième des concentrations maternelles24,25. Ces concentrations peuvent varier en fonction de la perméabilité et de la capacité biologique du placenta26. En outre, lorsque la marijuana est fumée, Les concentrations sériques de monoxyde de carbone chez la femme enceinte sont 5 fois plus élevées que celles du tabac, ce qui pourrait entraîner une altération des échanges gazeux respiratoires chez la mère et des effets néfastes sur le fœtus.27 Compte tenu de ces effets connus de la marijuana sur le placenta et son transport, Il est biologiquement plausible que la consommation de marijuana pendant la grossesse puisse affecter les résultats pour la mère et le fœtus.
Effets néfastes de la marijuana sur la grossesse et les nouveau-nés, les nourrissons, les enfants et les adolescents
Résultats pendant la période néonatale
Deux revues systématiques et méta-analyses récentes ont été publiées pour déterminer l'effet indépendant de la consommation de marijuana pendant la grossesse sur les résultats maternels et néonatals précoces. La première étude de Gunn et al28 a été utilisée pour examiner 24 études visant à déterminer l’effet de la consommation de marijuana sur l’anémie maternelle; les paramètres de croissance néonatale, tels que le poids à la naissance, le tour de tête et la longueur; admission à l'USIN; l'âge gestationnel; et naissance prématurée. Ils ont découvert que les femmes qui consommaient de la marijuana pendant la grossesse risquaient davantage de développer une anémie et que les nourrissons exposés à la marijuana avant la naissance présentaient une diminution du poids à la naissance (différence de poids moyenne de 110 g pour les nouveau-nés exposés et non exposés) et une probabilité plus grande d'avoir admission à une USIN. Ils n'ont trouvé aucune relation entre la consommation de marijuana et aucun de leurs autres résultats sélectionnés. Les auteurs ont toutefois souligné que l’incapacité de déterminer l’effet indépendant de la marijuana constituait une limite majeure de leur étude, car la plupart des études évaluées n’excluaient pas les personnes toxicomanes, y compris le tabac ou l’alcool, ou mesuraient la consommation de ces substances. substances. Les auteurs ont également cité d'autres limitations, telles que la manière dont l'utilisation de la marijuana était identifiée principalement par auto-évaluation, et peu des résultats évalués étaient normalisés dans toutes les études.
Conner et al ont tenté de remédier aux limitations citées dans l'analyse de Gunn et al28 en ajustant les effets de l'exposition au cannabis pendant la grossesse pour l'usage du tabac et d'autres facteurs de confusion, tels que l'usage d'autres drogues, dans la mesure du possible, dans une seconde méta-analyse. Leur étude comprenait la revue systématique de 31 études (de 1982 à 2015) dans lesquelles elle évaluait spécifiquement l'effet de la consommation maternelle de marijuana sur les issues néonatales comprenant un faible poids à la naissance (<2500 g), un accouchement prématuré (<37 semaines de grossesse), poids à la naissance, âge gestationnel à l'accouchement, admission à l'USIN, statut «petit pour l'âge gestationnel», mortinatalité, avortement spontané, faibles scores d'Apgar, décollement du placenta et mort périnatale.29 L'un des principaux atouts de cette analyse était l'inclusion de la cohorte. les études utilisées pour mesurer l'utilisation d'autres substances, telles que le tabac et d'autres drogues à usage récréatif, et les facteurs socio-économiques et démographiques permettant de contrôler ces facteurs de confusion et de déterminer le rôle indépendant de la consommation de marijuana. L'exposition à la marijuana a été définie comme toute quantité, fréquence ou durée durant la grossesse, évaluée par une auto-évaluation ou par des moyens objectifs, le cas échéant; les groupes de comparaison étaient des femmes qui n'avaient pas consommé de marijuana pendant leur grossesse. Lorsque les analyses contrôlaient la consommation de tabac concomitante, les femmes qui fumaient de la marijuana uniquement n'étaient pas à risque d'accouchement prématuré, mais celles qui fumaient du tabac et de la marijuana présentaient des taux d'accouchement prématuré plus élevés que celles qui n'utilisaient ni marijuana ni tabac. Ils ont également trouvé aucune relation indépendante entre la consommation de marijuana et le statut de petit pour l'âge gestationnel, le décollement du placenta, le besoin d'admission à l'USIN ou l'avortement spontané. Ils ont constaté que les femmes consommant de la marijuana pendant la grossesse étaient plus susceptibles d'accoucher et d'avoir un mort-né à la naissance, mais ces résultats n'étaient pas ajustés, car leur capacité analytique à fournir un risque relatif ajusté était limitée. taux pour ces résultats. Ils ont conclu que la consommation de marijuana par la mère pendant la grossesse n'était pas un facteur de risque indépendant pour plusieurs résultats, étant donné l'effet de confusion avec des facteurs tels que le tabagisme. Ils ont déclaré que «la fréquence croissante de la consommation de marijuana pendant la grossesse pouvait jouer un rôle dans le risque d'effets néonatals indésirables», mais ont averti que «les femmes qui consomment plus de marijuana sont également plus susceptibles de consommer de plus grandes quantités de tabac et d'autres drogues», ce qui pourrait ne pas être complètement pris en compte dans leur examen.
Les deux revues systématiques comprenaient des études de cohorte longitudinales utilisées pour fournir des données contrastées en termes d'effets indésirables chez les nourrissons exposés à la marijuana prénatale pendant la grossesse. Il s'agit notamment de l'étude prospective prénatale Ottawa (OPPS), une étude de cohorte longitudinale de familles à faible risque, de race blanche, à prédominance moyenne appartenant à la classe moyenne30,31; l'Étude sur les pratiques de santé maternelle et le développement de l'enfant (MHPCD), une étude de cohorte de femmes à haut risque et de statut socioéconomique inférieur, représentant à la fois des femmes blanches et afro-américaines32; l'étude Generation R, une étude basée sur la population des Pays-Bas14; et l'étude longitudinale Avon sur la grossesse et l'enfance réalisée au Royaume-Uni.33 les chercheurs de l'OPPS ont constaté une diminution de la durée de gestation de 0,8 semaine associée à une consommation importante de marijuana34,35. Les chercheurs de l'étude MPHCD ont découvert que le poids à la naissance était augmenté chez les nouveau-nés exposés à la marijuana au cours du troisième trimestre de la grossesse. 35 Dans l’étude Génération R, la croissance fœtale a été mesurée par échographie et les chercheurs ont découvert un effet indépendant de la consommation de marijuana, en plus de l’effet observé avec la consommation de tabac concomitante, sur la diminution de la croissance fœtale observée à partir du deuxième trimestre poids à la naissance, en particulier lorsque la consommation de marijuana a été commencée au début de la grossesse et s'est poursuivie tout au long de la grossesse. Toute la grossesse.14 L’étude Génération R a également été utilisée pour évaluer le rôle de l’usage paternel de marijuana, et aucune association indépendante avec la croissance fœtale n’a été constatée. Dans l'étude longitudinale Avon, Fergusson et ses collaborateurs33 ont établi un lien entre la consommation prénatale de marijuana et des naissances moins longues, un tour de tête plus petit et un poids inférieur à la naissance chez ceux qui déclaraient avoir consommé de la marijuana pendant la grossesse, par rapport aux femmes du groupe témoin qui n'en déclaraient pas la consommation.
Les auteurs d'une autre grande étude récente de cohorte basée sur la population ont découvert que la consommation de marijuana autodéclarée, sans utilisation concomitante de nicotine et / ou de tabac, n'était pas associée aux complications de la grossesse, à la naissance prématurée ou à des changements dans les résultats néonatals tels que les scores d'Apgar et la croissance. paramètres.36 Cependant, l’utilisation concomitante de marijuana et de tabac, comparée à l’usage de tabac seul, entraînait un risque accru de conséquences périnatales indésirables multiples, des taux plus élevés d’asthme et de prééclampsie maternels, de naissances prématurées et de nourrissons dont le nombre diminuait (<25 e centile) circonférence de la tête et diminution du poids à la naissance (<25e centile). Moins de 1% des 12 069 femmes de l'échantillon total ont déclaré avoir consommé de la marijuana, ce qui soulève des préoccupations quant à la représentativité de l'échantillon ou à la validité de l'autodéclaration
Un petit nombre d'études ont été utilisées pour évaluer le rôle de la marijuana dans les résultats non traités dans les 2 revues systématiques ci-dessus, tels que les résultats chez les prématurés, les résultats comportementaux du nouveau-né et les anomalies fœtales. Dotters-Katz et al37 ont publié une analyse de données secondaires sur un groupe de nouveau-nés prématurés nés avant 35 semaines de grossesse comparant les résultats néonatals de l'exposition prénatale à la marijuana par rapport maternel ou par dépistage de drogue (n = 138) à celle des nourrissons sans exposition à la marijuana ( n = 1732). Ils ont constaté que l'exposition prénatale à la marijuana n'avait pas d'effet préjudiciable sur le décès avant la sortie de l'hôpital, hémorragie intraventriculaire de grade 3 ou 4, leucomalacie périventriculaire, entérocolite nécrosante, dysplasie bronchopulmonaire, paralysie cérébrale et / ou un développement de Bayley - II <70 at 2 van Gelder et al38 ont constaté un taux plus élevé d'anencéphalie chez les fœtus de femmes qui fumaient de la marijuana immédiatement avant et pendant le premier trimestre de la grossesse, bien que les auteurs n'aient pas vérifié si ces femmes prenaient un supplément d'acide folique en début de grossesse. Parmi les comportements immédiats du nouveau-né observés chez les nourrissons exposés à la marijuana in utero, on peut citer une altération des schémas d'excitation, une régulation et une excitabilité, telles que mesurées par l'échelle de neurocomportemental du réseau NICU39. Des tremblements accrus et des réflexes de surprise prolongés et exagérés, mesurés par le L’évaluation comportementale chez les nouveau-nés a été observée au cours de la première semaine et a persisté entre 9 et 30 jours40. Une faible habituation et des réponses aux stimuli visuels mais non auditifs 41, des cris aigus anormaux 42 et des habitudes de sommeil anormales avec une diminution du sommeil calme une augmentation de la motilité du sommeil43 a également été observée au cours de la première semaine de vie. Une étude de Dreher et al44 sur des nourrissons jamaïcains exposés à la marijuana avant la naissance n'a révélé aucune anomalie. Les chercheurs ont suggéré que ces comportements partageaient certaines similitudes avec les symptômes observés dans le syndrome d’abstinence néonatale et avec le sevrage des opioïdes, mais aucune donnée n’est actuellement utilisée pour corroborer un syndrome de sevrage clinique avec exposition à la marijuana.
En résumé, les preuves des effets néfastes indépendants de la marijuana sur les résultats néonatals et le développement prénatal chez l'homme sont limitées, et une incohérence dans les conclusions peut être le résultat de la confusion potentielle causée par la forte corrélation entre la consommation de marijuana et l'utilisation d'autres substances telles que les cigarettes. et l’alcool, ainsi que des facteurs de risque sociodémographiques. Cependant, les preuves provenant des études de recherche disponibles indiquent un motif d'inquiétude, en particulier concernant la croissance fœtale et les comportements néonataux précoces.
Effets ultérieurs pendant l'enfance, l'adolescence et le début de l'âge adulte
Deux études longitudinales (l'OPPS et le MHPCD, décrites dans la section précédente) ont été utilisées pour observer des cohortes d'individus exposés avant la naissance, de la petite enfance à l'adolescence et au début de l'âge adulte, et fournissent la plupart des preuves limitées disponibles effets neurodéveloppementaux à long terme résultant de l'exposition prénatale à la marijuana.30,32 Les auteurs des deux études ont évalué les résultats à long terme dans les domaines de la fonction exécutive, de la cognition, des résultats scolaires et du comportement.
Les chercheurs de l'OPPS observent sa cohorte depuis 1978 (84 femmes enceintes qui consommaient de la marijuana) et ont démontré qu'indépendamment du tabac et des autres drogues, l'exposition à la marijuana avait des effets importants et omniprésents chez les enfants à partir de 4 ans. et continuer dans la jeunesse adulte. Les effets observables initiaux à 4 ans comprenaient des scores plus faibles en raisonnement verbal et en tâches de mémoire45. À 6 ans, les enfants exposés à la marijuana, comparés aux enfants non exposés du groupe témoin, présentaient des lacunes dans les mesures globales de la compréhension du langage, de la mémoire, fonctions visuelles et / ou perceptives, et tâches de lecture qui nécessitent une attention soutenue, avec une relation dose-réponse observée, en ce sens que les personnes exposées à des quantités plus élevées de marijuana présentaient un dysfonctionnement plus important sur des échelles impulsives et hyperactives46–48 ans entre 9 et 12 ans , l’exposition à la marijuana n’était pas associée de manière indépendante à l’intelligence globale ou aux sous-échelles verbales des tests d’intelligence, mais était associée à des déficits dans les tâches de la fonction exécutive, tels que le contrôle des impulsions et la résolution de problèmes visuels.49–52 De 13 à 16 ans, des problèmes ont été vus dans les domaines de l’attention, de la résolution de problèmes, de l’intégration visuelle et des compétences analytiques nécessitant une attention soutenue51,53–55. cette cohorte âgée de 18 à 22 ans a révélé des modifications de l'activité neuronale avec des tâches de mémoire de travail non observées chez les enfants appariés non exposés du groupe témoin56. Fried et al ont postulé que les problèmes de comportement et la baisse de performance des mesures globales observées tout au long de l'enfance début de l'âge adulte sont le reflet de déficits dans le fonctionnement de l'exécutif et non de l'intelligence générale31, 54, 57, 58
Les chercheurs du MHPCD ont observé une cohorte de nourrissons exposés depuis 1982 afin de déterminer les effets indépendants de la marijuana sur la cognition, le comportement, le tempérament, les troubles de la santé mentale et la toxicomanie dès la petite enfance, à l'adolescence et au début de l'âge adulte. À l'âge de 9 mois, on a observé un retard de développement mental59. À l'âge de 3, 4 et 6 ans, des déficits dans les tâches de la fonction exécutive similaires à ceux observés dans l'OPPS, avec une mémoire plus faible et des mesures verbales ont été trouvés60,61; à l'âge de 6 ans, une attention soutenue avec facultés affaiblies pour les tâches de vigilance et le raisonnement verbal a été observée et une impulsivité et une hyperactivité accrues ont été observées chez les personnes exposées au cours du premier trimestre dont les mères fumaient au moins 1 articulation par jour61. résolution visuelle de problèmes de 9 à 12 ans et augmentation de l'hyperactivité, de l'impulsivité et de l'inattention à 10 ans chez les mères dont la mère avait fumé de la marijuana durant les premier et troisième trimestres.62 Contrairement à l'OPPS, dont les auteurs n'ont pas constaté de déficit En ce qui concerne les capacités intellectuelles et les mesures de tests académiques standardisés entre 6 et 9 ans, entre 13 et 16 ans, les auteurs du MHPCD ont constaté des scores de lecture et d’orthographe plus faibles chez les enfants de 10 ans dont la mère a déclaré avoir fumé au moins une articulation par jour le premier trimestre de la grossesse et les déficits en compréhension à la lecture et en insuffisance de performance, tels que mesurés par le Wide Range Achievem Test d'évaluation – révisé, avec les mères qui ont déclaré avoir fumé de la marijuana au cours du deuxième trimestre62. Des scores globaux de performance globale en lecture, orthographe et mathématiques plus faibles ont également été observés à 14 ans63. Des mesures des comportements problématiques et des symptômes de santé mentale ont également été rapportés dans les deux études de cohorte. Les auteurs de l'OPPS ont constaté des taux plus élevés de comportements problématiques signalés entre 6 et 9 ans64 et des taux plus élevés de symptômes dépressifs entre 16 et 21 ans65. Les auteurs de la MHPCD ont également constaté des taux plus élevés de symptômes dépressifs et de comportements extériorisants entre parents et rapport de l'enseignant dans la cohorte exposée à l'âge de 10 ans et un risque accru de psychose chez les jeunes adultes.66,67 Des taux plus élevés de consommation de substances ont également été rapportés dans ces deux études de cohorte. Les auteurs de l'OPPS ont constaté une apparition plus précoce et une consommation accrue de marijuana et de tabac dans les cohortes exposées, observés entre 16 et 21 ans 65, et les auteurs de la MHPCD ont constaté des taux plus élevés de consommation de marijuana et de tabac chez les 14 à 21 ans. , même après prise en compte de l’environnement familial et de la consommation de substances psychoactives par les parents66,68, Sonon et al69 ont également démontré des taux plus élevés de consommation de marijuana chez les jeunes adultes après une exposition prénatale à la marijuana.
En résumé, il est essentiel de noter que les études décrites ci-dessus ont des limites qui peuvent menacer la validité des résultats. Par exemple, les études dans lesquelles les auteurs examinent les résultats proximaux, tels que les issues foetales ou néonatales précoces, reposent principalement sur l’autodéclaration de la consommation de marijuana, et il existe peu de normalisation entre la quantité de marijuana utilisée et la fréquence d’utilisation. . Un grand nombre de ces études incluaient des femmes enceintes qui utilisaient d'autres substances en plus de la marijuana, telles que le tabac, l'alcool ou d'autres drogues, et des méthodes analytiques étaient utilisées pour contrôler les effets de confusion de ces autres substances. Pour des résultats plus distaux, tels que la cognition et le comportement ultérieurs chez les enfants et les adolescents, les études ont été limitées sur les variables environnementales et sociodémographiques que les auteurs pouvaient contrôler, susceptibles d'influencer le développement de l'enfance et de l'adolescence70,71. le manque relatif de recherche dans ce domaine, les résultats concernant les variables de croissance72 et les résultats neurodéveloppementaux et comportementaux peuvent être utilisés pour suggérer que la consommation de marijuana pendant la grossesse pourrait ne pas être inoffensive. En outre, les études de cohorte existantes ont été menées lorsque la marijuana disponible avait une puissance beaucoup plus faible que celle disponible aujourd'hui, ce qui laisse craindre que les conséquences néfastes de l'exposition prénatale chez les femmes actuellement enceintes ne dépassent probablement pas ce qui a été rapporté à ce jour. 18 (Voir la section «Autres considérations» pour une discussion sur la puissance.) Des recherches rigoureuses sont nécessaires pour déterminer les effets indépendants de la marijuana, du tabac et d'autres drogues sur les conséquences néonatales et postérieures de l'enfance et de l'adulte.
Mécanismes utilisés pour expliquer les effets sous-jacents sur le fœtus en développement
Les cannabinoïdes atténuent leurs effets par le biais des récepteurs cannabinoïdes de types 1 et 2. Le système endocannabinoïde (ECS) comprend ces récepteurs, ainsi que les cannabinoïdes neurochimiques anandamide et 2-arachidonoylglycérol. Cela a été étudié à la fois chez des modèles animaux et humains, en particulier pour son effet sur le système immunitaire et le système nerveux central23. Bien que les conséquences de l'exposition prénatale à la marijuana chez les femmes enceintes, tant comportementales que développementales, ont été documentées dans des études épidémiologiques.
Relations du systeme endocannabinoide avec les autres neurotransmetteurs
Il a été constaté que le SCE (systeme endocannabinoide) avait une forte interaction avec les systèmes opioïdes, via les récepteurs opioïdes ?, ? et ? 80; Jutras-Aswad et al79 ont découvert qu'une exposition précoce à la marijuana avait une influence sur l'expression et l'activité des récepteurs opioïdes découverts. être important dans la récompense et les comportements de dépendance ultérieurs. L’ECS s’est également avéré associé aux systèmes sérotoninergique, adrénergique, glutamate et acide ?-aminobutyrique78.
Pour le clinicien
L'American Academy of Pediatrics (AAP), l'ACOG et l'American Society of Addiction Medicine recommandent que toutes les femmes qui envisagent une grossesse, les femmes enceintes tout au long de leur grossesse et celles qui assistent à des visites pédiatriques avant l'accouchement soient systématiquement dépistées pour usage de l'alcool et d'autres drogues, y compris la marijuana. , en utilisant un questionnaire de dépistage validé.17,81 Des techniques de dépistage et d’intervention brève sont recommandées pour conseiller l’abstinence des personnes qui utilisent des substances et pour orienter le traitement des personnes répondant aux critères de tout trouble lié aux substances 81. Malgré ces recommandations, dans une étude, Holland et coll82 ont constaté que sur les 19% de femmes déclarant avoir déjà consommé de la marijuana (53%) ou ayant déjà consommé de la marijuana lors de leur première visite prénatale, seules 52% avaient bénéficié de tout type de conseil. De plus, les conseils fournis portaient principalement sur les conséquences juridiques et protectrices de la détection lors de l'accouchement, plutôt que sur les effets médicaux ou sanitaires spécifiques de la consommation de marijuana. En juillet 2015, l'ACOG a publié un énoncé de position qui était spécifiquement utilisé pour déconseiller «la prescription ou la suggestion d'utilisation de la marijuana à des fins médicales pendant la période précédant la conception, la grossesse et l'allaitement» 5. La plupart des États qui ont légalisé la marijuana à des fins médicales ne l'ont pas spécifiquement limitée. distribution aux femmes enceintes. L'Oregon est le seul État à avoir légiféré pour que les femmes enceintes ou allaitantes aient des avertissements spécifiques aux points de vente pour les dispensaires83. Le présent rapport n'a pas pour objet de discuter de questionnaires validés spécifiques disponibles ni de divers moyens de procéder à un dépistage objectif.
Les fournisseurs de soins de santé ont pour mandat de signaler aux services de protection de l'enfance tout cas présumé de maltraitance ou de négligence envers un enfant. La loi de 2010 sur la maltraitance et le traitement des enfants ainsi que sur la prévention exige que tous les États disposent de politiques et de procédures pour signaler les nouveau-nés et autres enfants exposés à des substances illicites au sens de la définition de la maltraitance et / ou de la négligence. Étant donné que la marijuana est toujours une substance illicite au sens de la loi fédérale, cette loi s'applique à l'exposition à la marijuana dans tous les États, quel que soit le statut juridique de la consommation de marijuana par des adultes dans chaque État. Certains États peuvent avoir d’autres exigences en matière de déclaration des nouveau-nés exposés à des drogues et à d’autres expositions à des enfants84.
Compte tenu de ces exigences légales, il est conseillé à tous les prestataires de soins de santé qui voient des femmes enceintes de connaître les exigences de déclaration spécifiques de leur état et les conséquences juridiques et sociales néfastes potentielles de l'identification de la consommation de substances psychoactives chez leurs patients. Lorsqu'il existe une obligation légale ou médicale pour un prestataire de soins de santé de tester un patient, celui-ci doit informer les patients de ces conséquences potentielles avant de commander des tests de dépistage de drogue et faire un effort raisonnable pour obtenir un consentement éclairé5. le signalement des nouveau-nés exposés à la drogue, ils remplacent la loi fédérale sur la protection confidentielle des dossiers des patients recevant un traitement contre la toxicomanie (42 Code de réglementation fédérale, partie 2) .81
Allaitement et consommation de marijuana
L'allaitement est reconnu comme la méthode d'alimentation idéale pour les nourrissons en raison des nombreux avantages de l'allaitement à court et à long terme pour la mère et le nourrisson. Ces avantages incluent, sans toutefois s'y limiter, une diminution des infections, telles que la gastro-entérite, les otites et les maladies respiratoires graves; diminution de l'obésité et du diabète sucré; diminution du taux de syndrome de mort subite du nourrisson; amélioration du développement intellectuel; diminution des pertes sanguines post-partum; augmentation de l'espacement des naissances; et diminution du risque de diabète de type 2 chez la mère85.
Lorsque les mères enceintes prennent des médicaments prescrits ou à des fins récréatives, les avantages de l’allaitement doivent être pesés par rapport aux effets du médicament sur le nourrisson afin de prendre une décision conforme à son intérêt. De nombreux médicaments que les mères utilisent pendant l'allaitement sont également pris pendant la grossesse. Il peut être difficile de déterminer si les effets du médicament sur le nourrisson sont imputables à une exposition pendant la grossesse ou à l'allaitement. De plus, la capacité de la mère à prendre soin de son bébé peut être affaiblie à cause de sa consommation de marijuana. Les nourrissons peuvent également être exposés à la marijuana par inhalation de marijuana fumée en présence du nourrisson86,87.
Épidémiologie
Il existe peu de données sur la fréquence d'utilisation de la marijuana par les femmes pendant l'allaitement. Un rapport du Colorado, où la marijuana est légale pour certaines femmes, a interrogé des femmes participant au programme spécial de nutrition supplémentaire pour femmes, nourrissons et enfants du plus grand département de santé local de l'État. Elle a révélé que 7,4% des mères de moins de 30 ans et 4% des mères de plus de 30 ans consommaient déjà de la marijuana. Parmi tous les consommateurs de marijuana (passés, actuels, actuels), 35,8% ont déclaré en avoir consommé à un moment de la grossesse, 41% depuis la naissance du nourrisson et 18% en allaitant.88
Pharmacocinétique de la marijuana dans le lait maternel
L'excrétion des médicaments dans le lait maternel dépend de facteurs chimiques liés au médicament, notamment de l'ionisation, du poids moléculaire, de la solubilité dans les lipides et dans l'eau, ainsi que du pH du médicament. Le principal cannabinoïde psychoactif de la marijuana, le THC, est lié à 99% aux protéines, est soluble dans les lipides et a un poids moléculaire de 314.89. Il provoque également le stockage du THC dans des tissus remplis de lipides tels que le cerveau. On sait peu de choses sur les autres cannabinoïdes contenus dans la marijuana et leur transfert dans le lait maternel. Il existe peu de données sur le transfert de THC dans le lait maternel. Dans le tableau 1, nous énumérons les résultats des deux seules références principales sur les concentrations de THC dans le lait maternel. Ces données limitées de Perez-Reyes et Wall90 ainsi que de Marchei et al91 révèlent que le THC est transféré dans le lait maternel. Il n'y a aucune information sur la relation entre la quantité transférée et la concentration de THC dans la marijuana, la fréquence d'utilisation ou la concentration dans le plasma maternel.
L'effet de la marijuana sur les nourrissons nourris au sein
Tennes et al92, et Astley et Little93, deux petites études datant des années 1980, tentent d'évaluer l'effet de la consommation de marijuana chez la mère pendant l'allaitement chez le nourrisson. Les deux études incluaient des mères qui consommaient aussi de l'alcool, d'autres drogues et du tabac. Tennes et coll92 ont étudié 258 mères consommant de la marijuana et les ont comparées à des mères ne consommant pas de marijuana. Ils ont examiné les nourrissons âgés de 24 à 72 heures et un sous-groupe âgé de 1 an. Ils ont constaté les résultats suivants: (1) les consommateurs de marijuana étaient plus susceptibles de consommer des drogues illicites et de l’alcool, avec une relation dose-réponse linéaire significative entre la consommation de marijuana et l’alcool (R = 0,45; P <0,01); (2) les nourrissons exposés à la marijuana étaient légèrement plus courts; 3) la plupart des mères ont diminué leur consommation de marijuana pendant la grossesse; et (4) aucune différence n'a été constatée dans la croissance sur un an et les scores aux échelles de développement de Bayley; cependant, seuls 27 des nourrissons testés à l'âge d'un an ont été exposés à la marijuana tout en étant nourris au sein. Ces résultats sont limités par le petit nombre de nourrissons exposés à la marijuana par l'allaitement, par l'auto-sélection des mères ayant participé au suivi après un an et par le manque de contrôle de l'utilisation d'autres substances, notamment l'alcool92.
Astley et Little93 ont étudié le régime alimentaire, l'alcool et le tabac au cours de l'allaitement chez un groupe de mères de la classe moyenne. L'évaluation développementale à un an s'est achevée chez 68 nourrissons dont les mères utilisaient de la marijuana pendant l'allaitement et qui étaient jumelées à des mères présentant une consommation d'alcool et de tabac similaire et ne consommant pas de marijuana pendant l'allaitement. Parmi les mères allaitantes, 79% ont déclaré avoir consommé de la marijuana pendant la grossesse, par rapport à 15% des mères de nourrissons nourris au lait maternisé. Dans l’analyse de régression multivariée, l’exposition du nourrisson à la marijuana pendant l’allaitement au cours du premier mois était associée à une diminution de 14 ± 5 points des scores moteurs après contrôle de la consommation de tabac, d’alcool et de cocaïne pendant la grossesse et l’allaitement. La consommation de marijuana au cours du troisième mois de la vie n’a eu aucun effet pendant l’allaitement. La consommation de marijuana au cours du premier trimestre de la grossesse a faussé ces résultats, et il n'était pas clair si l'exposition avant la naissance ou pendant l'allaitement avait davantage d'association. Les études de Tennes et al92 et d’Astley et Little93 portaient sur des échantillons de petite taille. Elles ont été complétées il ya plus de 30 ans, étaient associées à la consommation de marijuana pendant la grossesse de la mère et n’avaient pas fait l’objet d’un suivi à long terme. Ces limitations rendent difficile la distinction entre les effets indépendants de la consommation de marijuana pendant l'allaitement et l'exposition prénatale.
Un autre sujet de préoccupation concerne l'utilisation du lait maternel exprimé pour l'alimentation du nouveau-né prématuré lorsque la mère a signalé une consommation de marijuana ou a obtenu des résultats de test positifs à la marijuana. Il a été démontré que le lait maternel exprimé améliorait considérablement les résultats chez les prématurés en diminuant le taux d’entérocolites nécrosantes (chirurgicales et non chirurgicales), en contribuant à la réalisation plus rapide d’aliments entaux complets, en diminuant le taux de sepsis et en améliorant les résultats neurodéveloppementaux, en particulier pour le développement. prématurés dont le poids à la naissance est inférieur à 1500 g.85
Recommandations publiées par d'autres organisations
L'énoncé de politique du PAA de 2012, «L'allaitement maternel et l'utilisation de lait humain», incluait les directives suivantes: «L'abus de substances maternelles n'est pas une contre-indication catégorique à l'allaitement». «Les drogues illicites telles que la PCP (phencyclidine), la cocaïne et le cannabis peuvent détectés dans le lait maternel et leur utilisation par les mères qui allaitent est préoccupante, en particulier en ce qui concerne le développement neurocomportemental à long terme du nourrisson et sont donc contre-indiqués 85. »Bien que cela ait été interprété par certaines organisations professionnelles comme indiquant que chez le parent qui consomme de la marijuana, Le choix d'allaiter est «contre-indiqué», ce n'était pas l'intention de cette déclaration. On suggère plutôt d'encourager la mère à allaiter tout en s'abstenant complètement de consommer de la marijuana ainsi que d'autres drogues, de l'alcool et du tabac. Ce poste a été soutenu par plusieurs autres organisations et ressources professionnelles. Par exemple, LactMed (une base de données consultable gratuitement de la National Library of Medicine) recommande que les mères soient encouragées à s'abstenir de consommer de la marijuana ou à réduire leur consommation pendant l'allaitement et à réduire au minimum l'exposition de leur mari à la fumée de marijuana. Le comité d’évaluation par les pairs LactMed, qui examine les données publiées pour en assurer la validité et l’actualité scientifiques, recommande de poursuivre l’allaitement au sein86. C’est similaire aux recommandations de l’ACOG, selon lesquelles «Il n’existe pas suffisamment de données pour évaluer les effets de la consommation de marijuana sur les bébés l’allaitement et l’allaitement, et en l’absence de telles données, la consommation de marijuana est déconseillée. »5 L’Academy of Breastfeeding Medicine déclare:« Il est recommandé de recommander de s’abstenir de toute consommation de marijuana. À l'heure actuelle, bien que les données ne soient pas suffisamment fiables pour recommander de ne pas allaiter avec une consommation de marijuana, nous vous recommandons de faire preuve de prudence. "94 Après la légalisation de la consommation de marijuana par des adultes de 21 ans et plus, le Département de la santé publique et de l'environnement du Colorado a mis au point matériel sur la consommation de marijuana pendant la grossesse et l'allaitement. Ces supports incluent des documents d’éducation des patients pouvant être utiles aux pédiatres et aux familles. Ils sont disponibles à l’adresse suivante: www.colorado.gov/pacific/sites/default/ … Pregnancy- Breastfeeding-Clinical-Guidelines.pdf. D'autres États qui ont légalisé la marijuana peuvent avoir des informations pédagogiques similaires pour les prestataires de soins de santé et les familles.
Autres considérations
La puissance de la marijuana actuellement disponible est bien supérieure à celle disponible il y a une décennie. La puissance du THC dans les échantillons étudiés en 1983 était en moyenne de 3,2% et la moyenne en 2008 de 13,2%; Les auteurs de la même étude ont identifié des échantillons isolés avec des teneurs en THC atteignant 27,3% et 37,2% 95. Ces puissances plus élevées ainsi que les nouvelles pratiques de consommation de marijuana, telles que tamponner ou vaporiser, peuvent augmenter de manière significative la concentration de THC consommé. Des études ont révélé que le développement de souches de marijuana avec des concentrations de THC plus élevées a réduit la concentration de cannabidiol, diminuant éventuellement les avantages médicinaux pour un certain nombre de conditions. Outre le THC et le cannabidiol, la plante de marijuana contient de nombreuses autres substances dont on sait peu de choses. De plus, la marijuana est souvent cultivée à l'aide de pesticides, d'herbicides, de rodenticides et d'engrais, dont beaucoup sont toxiques.96,97. L'exposition à la marijuana peut également exposer le fœtus et le nourrisson à ces toxines.
autres considérations
La puissance de la marijuana actuellement disponible est bien supérieure à celle disponible il y a une décennie. La puissance du THC dans les échantillons étudiés en 1983 était en moyenne de 3,2% et la moyenne en 2008 de 13,2%; Les auteurs de la même étude ont identifié des échantillons isolés avec des teneurs en THC atteignant 27,3% et 37,2% 95. Ces puissances plus élevées ainsi que les nouvelles pratiques de consommation de marijuana, telles que tamponner ou vaporiser, peuvent augmenter de manière significative la concentration de THC consommé. Des études ont révélé que le développement de souches de marijuana avec des concentrations de THC plus élevées a réduit la concentration de cannabidiol, diminuant éventuellement les avantages médicinaux pour un certain nombre de conditions. Outre le THC et le cannabidiol, la plante de marijuana contient de nombreuses autres substances dont on sait peu de choses. De plus, la marijuana est souvent cultivée à l'aide de pesticides, d'herbicides, de rodenticides et d'engrais, dont beaucoup sont toxiques.96,97. L'exposition à la marijuana peut également exposer le fœtus et le nourrisson à ces toxines.
Conclusions et Recommendations
Les pédiatres occupent une position privilégiée pour conseiller les femmes en âge de procréer sur les conséquences négatives potentielles de la consommation de marijuana pendant la grossesse et l'allaitement. Discuter de ce que l'on sait des conséquences néfastes de la consommation de marijuana pendant la grossesse et l'allaitement lors des visites prénatales avec le pédiatre ou le prestataire d'obstétrique est un élément important pour la promotion des meilleurs résultats en matière de santé pour la femme enceinte et le bébé. La légalisation de la marijuana peut donner la fausse impression que la marijuana est sans danger. En raison de préoccupations éthiques, il n’existe pas d’essais contrôlés randomisés sur les effets de la consommation de marijuana chez les femmes enceintes ou allaitantes, et les études longitudinales disponibles doivent être considérées avec prudence, étant donné que l’effet de la marijuana pendant la grossesse peut être confondu avec d’autres substances licites et illicites et facteurs de risque sociodémographiques et environnementaux. Cependant, les données épidémiologiques et animales disponibles soulèvent des préoccupations concernant à la fois la croissance à court terme et les conséquences neurodéveloppementales et comportementales à long terme de l'exposition prénatale à la marijuana. Notre compréhension actuelle de l'ECS et de son rôle dans le développement des circuits neuronaux au début de la vie fœtale fournit également une «justification théorique» du potentiel des substances de la marijuana, en particulier du THC, à affecter le développement neurologique.18
L'allaitement présente de nombreux avantages précieux pour la santé de la mère et du nourrisson, en particulier du prématuré. Des données limitées révèlent que le THC est effectivement transféré dans le lait maternel et il n'existe aucune preuve d'innocuité ou de danger de la consommation de marijuana pendant l'allaitement. Par conséquent, les femmes doivent également être informées des connaissances relatives aux effets néfastes du THC sur le développement du cerveau pendant la petite enfance, lorsque la croissance et le développement du cerveau sont rapides.
L'importance des résultats publiés et de la recherche émergente concernant les effets négatifs potentiels de la marijuana sur le développement du cerveau est préoccupante malgré les recherches limitées et constitue la base des recommandations suivantes:
** Les femmes qui envisagent une grossesse ou qui sont en âge de procréer doivent être informées du manque de recherches définitives et informées des préoccupations actuelles concernant les effets néfastes potentiels de l’utilisation de THC sur la femme et sur le développement du fœtus, du nourrisson et de l’enfant. La marijuana peut être incluse dans le cadre d’une discussion sur l’usage du tabac, de l’alcool et d’autres drogues et médicaments pendant la grossesse.
** Dans le cadre des conseils d'anticipation de routine et du conseil en matière de contraception, il est important d'informer tous les adolescentes et les jeunes femmes que, si elles tombent enceintes, la marijuana ne doit pas être utilisée pendant la grossesse.
** Les femmes enceintes qui utilisent de la marijuana ou d'autres produits contenant des cannabinoïdes pour traiter un état pathologique ou pour traiter les nausées et les vomissements pendant la grossesse doivent être informées du manque de données de sécurité et des effets néfastes possibles du THC dans ces produits sur le fœtus en développement. à leur fournisseur de soins de santé pour des traitements alternatifs offrant de meilleures données de sécurité spécifiques à la grossesse.
** Les femmes en âge de procréer qui sont enceintes ou envisagent de devenir enceintes et qui sont identifiées par le dépistage universel comme consommant de la marijuana devraient être conseillées et, comme indiqué cliniquement, subir une intervention brève et être dirigées vers un traitement.
** Bien que la marijuana soit légale dans certains États, les femmes enceintes qui en font usage peuvent faire l'objet d'enquêtes en matière de protection de l'enfance si le résultat de leur dépistage de la marijuana est positif. Les prestataires de soins de santé doivent souligner que le but du dépistage est de permettre le traitement de la toxicomanie de la femme, et non de la punir ou de la poursuivre.
** Les données actuelles sont insuffisantes pour évaluer les effets de l'exposition des nourrissons à l'utilisation de marijuana par la mère pendant l'allaitement. En conséquence, la consommation de marijuana par la mère pendant l'allaitement est découragée. Les risques potentiels d'exposition des nouveau-nés aux métabolites de la marijuana étant inconnus, les femmes devraient être informées du risque potentiel d'exposition pendant l'allaitement et encouragées à s'abstenir de consommer des produits contenant de la marijuana pendant l'allaitement.
**Les femmes enceintes ou qui allaitent devraient être averties de l'exposition des nourrissons à la fumée de marijuana dans l'environnement, compte tenu des nouvelles données sur les effets de la fumée de marijuana passive.
** Les femmes qui se sont abstenues d'une précédente consommation de marijuana devraient être encouragées à le faire pendant la grossesse et l'allaitement.
** Des recherches supplémentaires sur l'utilisation et les effets de la marijuana pendant la grossesse et l'allaitement sont nécessaires.
** Les pédiatres sont priés de collaborer avec leurs services de santé nationaux et / ou locaux si la légalisation de la marijuana est envisagée ou s'est déjà produite dans leur pays afin de contribuer à une politique et à une éducation constructives et non punitives pour les familles.
Dernière modification par prescripteur (28 novembre 2019 à 15:54)
S'il n'y a pas de solution, il n'y a pas de problème. Devise Shadok (et stoicienne)
Hors ligne

- prescripteur
- Adhérent PsychoACTIF
- Inscrit le 22 Feb 2008
- 12631 messages
- Blogs
S'il n'y a pas de solution, il n'y a pas de problème. Devise Shadok (et stoicienne)
Hors ligne
C'est indéniable que c'est à ce moment là qu'il y a pas mal de choses qui se développent, mais il me semble d'avoir lu des études aussi que la "qualité" du sperme des fumeurs...je dis ça parce que juste ces campagnes de santé publique font porter tout le poids et la culpabilités aux femmes (et les femmes UD en reçoivent une double couche).
Du coup, même si je suis pour développer des vraies connaissances qui permettent à la grossesse de se passer dans la meilleur des façon et de donner le max de chances aux futurs humains, je suis quand même contre une culpabilisation hygiéniste et moralisatrice des femmes en tant que génitrices.
Sans compter, qu'une des caractéristiques principales des humains par rapport à tant d'autres animaux c'est le fait que le cerveau se développe, bien plus que dans d'autres espèces, après la naissance. Ce qui veut dire que tous ces études ne prennent pas en compte , par exemple, le tabagisme ou la fumée de cannabis "passive" qu'un nouveau née peut "subir" par son environnement (c'est à dire pas seulement la mère, mais éventuellement le père aussi !!). Difficile d'évaluer des résultats à la 4eme, 7eme et 10eme année en mettant la baisse des résultats que sur les 9 mois dans le ventre maternel (alors qu'il y a bien plus de temps "à l'extérieur").
https://www.cairn.info/revue-spirale-20 … ge-17.htm#
Pierre Changeux, L'homme neuronal
Désolée pour le coup de gueule, mais je crois vraiment important de développer une recherche sérieuse qui ne finit juste par culpabiliser et moraliser encore plus le comportement des femmes !!
EDIT : je vois qu’entre-temps prescripteur a justement publié un étude où c'est dit :
Comme quoi, sans sous-évaluer les effets pendant la grossesse, il faut penser aussi à l'après...(et là c'est souvent une responsabilité partagé entre les parents + environnement en général)...
Dernière modification par cependant (28 novembre 2019 à 17:09)
fugu kuwanu hito niwa iwaji
Hors ligne

- prescripteur
- Adhérent PsychoACTIF
- Inscrit le 22 Feb 2008
- 12631 messages
- Blogs
 ), faut il pour autant ne pas porter à la connaissance du public les articles documentés comme celui que j'ai traduit ?
), faut il pour autant ne pas porter à la connaissance du public les articles documentés comme celui que j'ai traduit ?Pour moi tes mises en garde sont pertinentes mais il faut aussi donner l'information du moment.
Amicalement
S'il n'y a pas de solution, il n'y a pas de problème. Devise Shadok (et stoicienne)
Hors ligne
prescripteur a écrit
Mais, Cependant (
), faut il pour autant ne pas porter à la connaissance du public les articles documentés comme celui que j'ai traduit ?
Pour moi tes mises en garde sont pertinentes mais il faut aussi donner l'information du moment.
Amicalement
Si, si carrément (d'ailleurs super travail de traduction !) mais juste voilà je pense que c'est important de contrebalancer (comme d'ailleurs le fait cet article aussi) pour ne pas tomber dans la moralisation plus que de la vraie RdR...
merci pour ton travail de diffusion et vulgarisation :)
fugu kuwanu hito niwa iwaji
Hors ligne
Je veux bien parler d'effets tératogène de certains ttt pour l'épilepsie, ils sont avérés, c'est pour cela que la depakine ou autres ne doivent pas être prescrits à des femmes susceptibles d'attendre un enfant.
Produit par le laboratoire Sanofi depuis 1967, l'antiépileptique Dépakine est sur la sellette car son principe actif est susceptible de provoquer dans 10% des malformations congénitales et de l'autisme et de retards intellectuels dans 40% des cas.25 août 2016
Pour le CBD il n'y a pas vraiment d'études aussi précises. Sauf que c'est maintenant un médicament qui a prouvé son efficacité là où des traitements de cheval ne donnaient pas de résultats probants... Des enfants qui sont ou seront parfois lourdement handicapés faute de CBD.
L'Agence nationale de sécurité du médicament a adressé, en décembre 2014, un courrier aux professionnels de santé pour leur rappeler les risques liés au valproate et ses dérivés (Dépakine®, Dépakote®, Dépamide®, Micropakine® et génériques). Ces médicaments anti-épileptiques ou prescrits à des personnes souffrant de troubles bipolaires comportent un risque pour les enfants exposés un utero. Selon l'Ansm, ces enfants "présentent un risque élevé de troubles graves du développement (jusqu'à 30 à 40% des cas) et/ou de malformations congénitales (environ 10% des cas)".
Si les consommateurs de cannabis avaient autant de soucis même en fumant avec du tabac, on le saurait depuis longtemps.
Les études à charge ont toujours eu des financement.
Prudence OK. Mais faut prendre un peu de distance avec la ribambelle de chercheurs français financés par des labos qui produisent les best sellers.
EDIT : c'est pas ce papier mais c'est mieux que rien, une vieille réf sur l'influence génétique du cannabis :
Vieux papier et hors sujet, le cannabis fumé ou pas n'est pas du CBD.
Et le cannabis moderne contient moins de CBD qu'une plante marocaine par exemple, le cannabis moderne n'en contient plus sur le marché noir... Ou de moins en moins, même sur ce qui est produit au Maroc.
Je connais pas mal de marocains assez âgés qui détiennent un savoir sans aucune étude scientifique. Tous disent que l'herbe le kiff ou le hash de l'herbe des occidentaux rend fou contrairement aux variétés anciennes...
Plutôt d'alarme sur le CBD dans une crise d'hygiènisme ou des lendemains de formation médicale à la française, je pense que le CBD doit être vu comme un vecteur de RDR y compris pour les femmes enceintes qui consomment du cannabis.
Dernière modification par Mister No (28 novembre 2019 à 21:48)
Just say no prohibition !
Hors ligne
Rosetemple a écrit
Peux-tu étayer ou expliquer ça s'il te plait ? Qu'est-ce que le D2R et en quoi est-ce lié à une vulnérabilité à la "toxicomanie"?
Bien sûr pas de soucis ! :)
A) Le "D" signifie qu'on parle d'un récepteur dopaminergique.
B) Le "2" signifie que c'est un sous-récepteur de type 2 c'est à dire un auto-récepteur et surtout celui le plus impacté dans une majorité de psychotropes.
Les récepteurs dopaminergiques sont impliqués dans plusieurs processus neurologiques, dont la motivation, le plaisir, la cognition, la mémoire, l'apprentissage et la motricité fine, ainsi que la modulation de la signalisation neurendocrine. Une signalisation anormale des récepteurs et des fonctions nerveuses de la dopamine est impliquée dans plusieurs troubles neuropsychiatriques.
Les psychostimulants sont des agonistes des récepteurs dopaminergiques.
Il y a cinq sous-types aux récepteurs de la dopamine, D1, D2, D3, D4 et D5.
Il y a également des éléments de preuve qui tendent à prouver l’existence possible des récepteurs D6 et D7, mais rien jusqu’à maintenant ne peut le confirmer de façon formelle.
Voilà pour définir un peu la chose. Maintenant pour répondre à ta question : Quel est le rapport ou le lien avec la toxicomanie ?
Il faut savoir que dans n'importe quelle addiction chronique tu épuises ta dopamine dans deux régions sous-corticales. C'est un neurotransmetteur qui te permet de prendre des décisions, d'être motiver pour tel ou tel action, de ressentir tel ou tel plaisir. J'essaye de faire simple pour pas te perdre mais c'est vrai que c'est un peu compliqué et qu'il faut bien suivre.
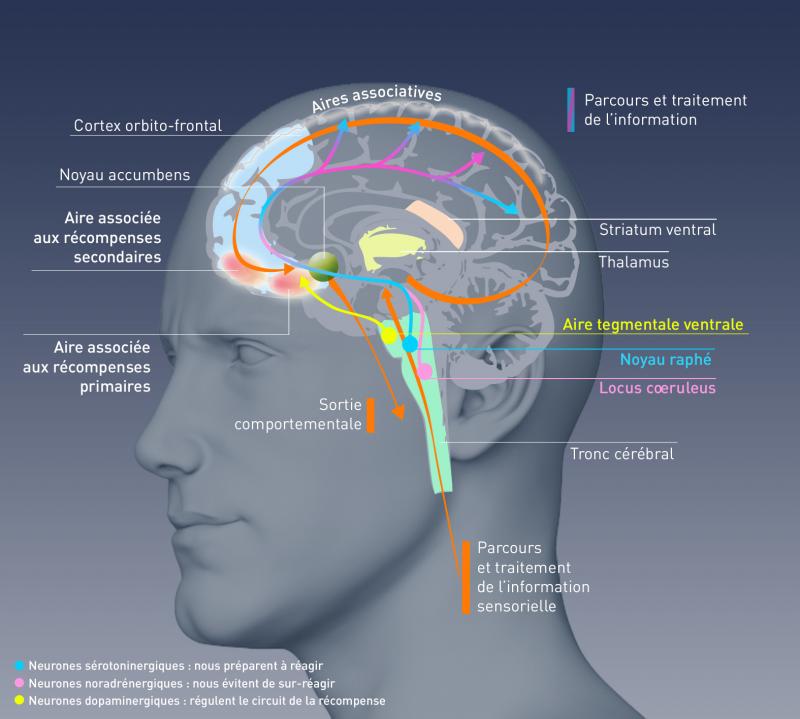
Si tu n'as plus beaucoup de dopamine ou de récepteurs permettant de l'accueillir, la conséquence c'est que tu auras plus de difficulté à ressentir le plaisir lié aux activités et événements de ta vie de tous les jours. Un enfant qui nait avec une raréfaction de récepteurs D2, aura tendance à chercher quelque chose capable de le satisfaire, et dans son cas on finira avec une vulnérabilité aux addictions.
Informations supplémentaires pour conclure :
Les stimulants (cocaïne, amphétamine, méthylphénidate, etc.) augmentent artificiellement et directement ton taux de dopamine via ces récepteurs.
Les opiacés, c'est pareille, la seule différence c'est qu'ils augmentent ton niveau de dopamine indirectement par une libération d'opioïdes en amont via les récepteurs mu, kappa, delta.
Le LSD, la MDMA, le tabac, l'alcool, le cannabis, etc. c'est encore une fois le même principe. Ils augmentent ton niveau de dopamine, indirectement comme pour les opiacés. Mais cette fois par une libération en amont de neurotransmetteurs comme la sérotonine ou le GABA.
Pour avoir une vue d'ensemble je te partage ce graphique qui résume ce que j'ai expliquer plus haut :

J'espère avoir été clair et compréhensif mais n'hésites pas à me dire si un point te paraît encore obscure. J'ai délibérément omis certaines informations et simplifiés d'autres parce que la neuroanatomie reste une discipline très complexe et je voulais vraiment éviter de perdre le lecteur.
pierre a écrit
Ca fait des affirmations gratuites qui n'avance pas à grand chose au final.
Tout ça pour dire qu'à l'instar du discours "on ne doit pas diaboliser les drogues dites dures", et je suis tout à fait d'accord, on ne doit pas banaliser le cannabis et partir du principe que c'est une plante psychoactive innofensive. Du simple fait qu'on parle de drogue douce dans les médias.
Je dis ça pour les commentaires que j'ai pu lire au dessus. Je pense que c'est important de nuancer.
De considérer que la plante est composée de molécules avec un potentiel thérapeutique tout en acceptant les études scientifiques démontrant un risque génétique pour la descendance de la femme enceinte.
Parce qu'il ne s'agit pas de mon opinion, ou de l'avis des médecins pour reprendre le terme "d'affirmations gratuites". Nan là on parle d'une méta-analyse scientifique sur des milliers d'américaines.
J'aimerais conclure sur le fait qu'il ne s'agit pas de pointer du doigt qui que ce soit. Seulement d'informer le grand public pour qu'il puisse prendre ses propres décisions en connaissance de cause 
Faites attention à vous et je vous souhaite un bon week-end 
Dernière modification par Heashka (29 novembre 2019 à 13:52)
Je cours entre l'hôpital, le laboratoire et les services neuropsychiatriques quand je ne suis pas en conférence à la faculté de médecine pour écouter l'actualité sur l'addictologie.
Hors ligne

- Rosetemple
- Drogologue

- Inscrit le 18 May 2019
- 157 messages
- Blogs
Heashka a écrit
A) Le "D" signifie qu'on parle d'un récepteur dopaminergique.
B) Le "2" signifie que c'est un sous-récepteur de type 2 c'est à dire un auto-récepteur et surtout celui le plus impacté dans une majorité de psychotropes.
Si tu n'as plus beaucoup de dopamine ou de récepteurs permettant de l'accueillir, la conséquence c'est que tu auras plus de difficulté à ressentir le plaisir lié aux activités et événements de ta vie de tous les jours. Un enfant qui nait avec une raréfaction de récepteurs D2, aura tendance à chercher quelque chose capable de le satisfaire, et dans son cas on finira avec une vulnérabilité aux addictions.
Ok, je vois. Merci beaucoup pour le temps passé à clarifier tout ça ! 
Dédicace à mon amie T'Etoile, la plus gentille et mignonne des personnages magiques !
Hors ligne

Tout ça pour dire qu'à l'instar du discours "on ne doit pas diaboliser les drogues dites dures", et je suis tout à fait d'accord, on ne doit pas banaliser le cannabis et partir du principe que c'est une plante psychoactive innofensive. Du simple fait qu'on parle de drogue douce dans les médias.
Tout à fait d'accord, mais tu ouvres un sujet pour mettre en garde les femmes enceintes sur le CBD et tu finis par une campagne madness reefer sur le potentiel additif du cannabis. 
https://fr.m.wikipedia.org/wiki/Reefer_Madness
Personne ne dit ici que le cannabis est une drogue qui n'est pas sans danger car naturelle ou ce genre de propos qui ont le don aussi de m'irriter. 
Pour en revenir au sujet, l'action du CBD sur le système de la dopamine semble peu propice au mécanisme de l'addition.
Les effets du CBD ne semblent pas dépendre de l'antagonisme des récepteurs de la dopamine.
Donc pour moi, le CBD ne représente pas un risque d'addiction et je ne suis pas le seul,le CBD n'est même pas une substance contrôlée bien que le principe actif d'un médicament.
Faut pas confondre le cannabis avec le CBD, c'est bien toi qui a ouvert un topic sur le CBD, non ? 
L'appel à la prudence dans ce cadre paraît plus facile à conditions que l' amalgame ne soit pas fait entre une teinture only CBD et du cannabis fumé censé en contenir... Le consommateur lambda risque de prendre cet appel à la prudence à une forme d'éxageration des méfaits supposés et en matière de cannabis, c'est pire qu'un coup d'épée dans l'eau. Plus personne n'écoute ou presque.
Pour en revenir aux effets tératogènes, on va vite finir par savoir si le CBD l'est ou pas contrairement à la plupart des anti épileptiques sur le marché.
Avec la spécialité de Gw pharma et les retours sur le moyen et long terme, on va enfin obtenir des données plus amples et on en a déjà je crois pour des interactions et surtout comment réguler... diminuer d'autres traitements comme pour le syndrome de Dravet.
Après perso, de ce que j'ai vu autour de moi en un demi siècle, je n'ai pas constaté heureusement que les consommateurs de cannabis faisaient des monstres littéralement.
Des consommateurs de CBD, j'en ai jamais croisé ou juste mon père. 
Mais c'est juste une interprétation de mon vécu...
En revanche il y a bien longtemps que l'on sait que les antiepileptiques ont souvent des effets tératogènes.
Ça c'est certain et très fréquent pour certain.
Dernière modification par Mister No (02 décembre 2019 à 22:20)
Just say no prohibition !
Hors ligne
- Psychoactif
- » Forums
- » Paroles de femmes
- » Prévention Grossesse et CBD - effets tératogènes et héréditaires
1
Sujets similaires dans les forums, psychowiki et QuizzZ
 |
5 | |
 |
[ Forum ] Grossesse et tramadol
|
1 |
 |
[ Forum ] Tramadol et grossesse
|
16 |
 0
0 0
0 0
0

 Soutenez PsychoACTIF
Soutenez PsychoACTIF